
分析 铜、银不能和稀硫酸反应,锌和稀硫酸反应生成硫酸锌和氢气,根据反应的化学方程式和提供的数据可以进行相关方面的计算和判断.
解答 解:(1)因为锌能和稀硫酸反应,因此能测量出铜的质量分数的是Cu-Zn合金.
故填:Cu-Zn.
(2)设锌的质量为x,反应的硫酸质量为y,
Zn+H2SO4═ZnSO4+H2↑,
65 98 2
x y 0.4g
$\frac{65}{x}$=$\frac{98}{y}$=$\frac{2}{0.4g}$,
x=13g,y=19.6g,
该合金中铜的质量分数是:$\frac{65g-13g}{65g}$×100%=80%,
答:该合金中铜的质量分数是80%.
(3)小华所用稀硫酸溶液中溶质的质量分数为:$\frac{19.6g}{100g}$×100%=19.6%,
答:小华所用稀硫酸溶液中溶质的质量分数为19.6%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 钙是维持人体正常功能所必需的元素.如图所示为“迪巧”钙片说明书的一部分.取5片钙片,放入 有50g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反应).烧杯内物质质量变为57.8g.试计算:
钙是维持人体正常功能所必需的元素.如图所示为“迪巧”钙片说明书的一部分.取5片钙片,放入 有50g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反应).烧杯内物质质量变为57.8g.试计算:查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. |  向一定体积HCl溶液中滴加NaOH溶液 | |
| B. | 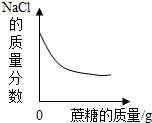 一定温度下,向一定量饱和NaCl溶液中不断加入蔗糖 | |
| C. | 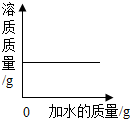 向饱和NaCl溶液中不断加水 | |
| D. |  向CuCl2和H2SO4的混合溶液中加入过量Ba(OH)2溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 化学调研小组的同学用氢氧化钠和稀盐酸探究中和反应,请你参与以下探究:
化学调研小组的同学用氢氧化钠和稀盐酸探究中和反应,请你参与以下探究:| 实验方法 | 可能观察到的现象 | 结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 一定质量的镁条在氧气中完全燃烧后生成氧化镁.固体质量随时间的变化关系如图所示.下列说法不正确的是( )
一定质量的镁条在氧气中完全燃烧后生成氧化镁.固体质量随时间的变化关系如图所示.下列说法不正确的是( )| A. | 生成MgO的质量:m2g | |
| B. | 参加反应的Mg的质量:m1 g | |
| C. | 参加反应的O2的质量:(m2-m1)g | |
| D. | 参加反应的镁和氧气的质量比:m1:(m2-m1)=3:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com