
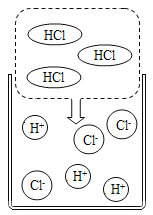
【题目】(1)如图是某同学査阅的氯化氢气体溶于水的示意图。从微观角度分析氯化氢气体不显酸性的原因是_____________。
(2)用硫酸铜配制农药波尔多液,溶解硫酸铜时不宜用铁制容器。用化学方程式表示其原因:___________。
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:初中化学 来源: 题型:
【题目】如图装置可以以完成多个简单实验,具有药品用量少、实验现象明显、尾气 不外逸等优点。

(1)若甲中吸有浓氨水,乙中吸有无色酚酞溶液,将甲、乙中的液体同时挤出,一段时 间后,可观察到挤入到烧杯②中的无色酚酞溶液______,说明分子具有的性质是______
(2)若先将甲中的液体挤出,观察出气球明显鼓起,一段时间后恢复原状,再将乙中的液体挤出,气球又明显鼓起,过一会略缩小,但不会恢复到原状,请将下表中的试剂补充完整。
滴管甲 | 烧杯① | 滴管乙 | 烧杯② | |
试剂 | H2O | ______ | ______ | Mg |
图示气球鼓起是因为装置内气压增大,第二次气压增大的原因是______。
(3)若甲中吸有水,乙中吸有稀硫酸,烧杯①中盛有用石蕊溶液染成紫色的干燥纸花,烧杯②中盛有碳酸钠 粉末,为了验证使石蕊变色的物质是碳酸而不是二氧化碳,应进行实验操作的是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组将等质量的锌、铁、铜三种金属粉末分别加入等质量、相同质量分数的稀硫酸中,观察到铜与稀硫酸无反应,测得锌、铁与稀硫酸反应产生气体体积与时间的关系如下图所示,关于该小组的实验有下列说法,其中正确的是( )
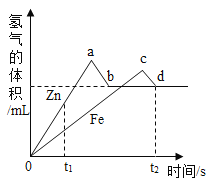
A.从t1时间就可以得出金属活动性:Zn>Fe>Cu
B.一定时间内气体体积从a降到b说明装置气密性不好
C.a>c是说明Zn生成的氢气比Fe多
D.反应结束后Fe一定剩余,Zn可能剩余
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸亚铁铵((NH4)2SO4·FeSO4·6H2O)俗称摩尔盐,可用于净水和治疗缺铁性贫血。工业上常利用机械加工行业产生的废铁屑(含有少量杂质 Fe2O3)为原料制备(如图)。
某化学兴趣小组拟用下列方案制备硫酸亚铁铵并进行相关探究。 查阅资料:
(1)FeSO4易被氧气氧化为Fe2(SO4)3,影响硫酸亚铁铵的等级。
(2)在FeSO4溶液中加入(NH4)2SO4固体可制备硫酸亚铁铵晶体,该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
(3)在0~60℃时,硫酸亚铁铵的溶解度比硫酸铵、硫酸亚铁的溶解度小,冷却混合液至室温便析出硫酸亚铁铵。
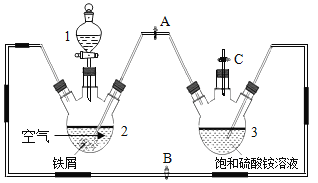
(探究一)用如上图所示装置制备硫酸亚铁铵。实验步骤如下:
①制备 FeSO4溶液:先关闭止水夹 A,再打开止水夹 B和 C,从分液漏斗滴加稀硫酸至三颈烧瓶2中,此装置中发生的化学反应主要有(用化学方程式表示)______、_______和![]() 。该过程中氢气的作用是______。
。该过程中氢气的作用是______。
②待装置中的铁屑快反应完时,关闭止水夹_______,打开止水夹_______,观察到的现象是_______。实验时为防止三颈烧瓶2中剩余铁屑通过导管进入三颈烧瓶3中,可采取的措施 是_______。
③放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵晶体,从中获得硫酸亚铁铵晶体的主要实验操作为过滤、洗涤、干燥。为洗涤(NH4)2SO4·FeSO4·6H2O 粗产品,下列方法中最合适的是______。
A 用冷水洗 B 先用冷水洗,后用无水乙醇洗
C 用 30%的乙醇溶液洗 D 用 90%的乙醇溶液洗
(探究二)探究硫酸亚铁铵样品的纯度取5g硫酸亚铁铵晶体溶于50mL水配成溶液,等分成两份,分别进行实验。
方案一:![]()
(1)实验中加入过量BaCl2溶液的目的______。
(2)利用方案一测得的数据,计算该硫酸亚铁铵样品的纯度(列出具体计算步骤)。((NH4)2SO4·FeSO4·6H2O的相对分子质量:392)__________
方案二:如图所示,向另一份中加入过量的NaOH溶液,充分反应后得到NH3
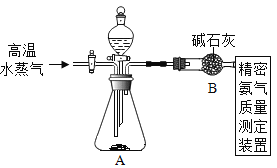
(3)(NH4)2SO4与NaOH反应的化学方程式为_______。
(4)实验中需不断通入高温水蒸气,其作用是_______。
(5)在实际测量中,利用方案二测得的样品纯度总是低于方案一测得的数值,可能的原因是______。
(探究三)对硫酸亚铁铵((NH4)2SO4·FeSO4·6H2O)晶体进行热重分析,温度与TG%的关系如下图所示
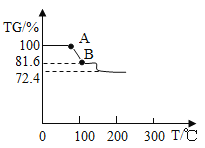
已知:温度低于 200℃,只有结晶水失去。
已知:TG% =![]()
TG%从 100%降低为 72.4%时,发生反应的化学方程式是_______ 。试计算AB段物质的化学式______________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属及金属材料由于具有优良的性能,在生产和生活中发挥着极其重要的作用,种类繁多的金属材料已成为社会发展的重要物质基础。
(1)人类文明与金属材料的发展应用关系密切,下列三种金属中,使用年代最久远的是_____填序号)。
①铁 ②铝 ③铜
(2)铁是全世界目前应用最为广泛的金属,如汽车、轮船的外壳都是铁制品,但每年因钢铁生锈造成的损失约占钢铁生产总量的三分之一,请写出一种防止钢铁生锈的措施__________。
(3)生铁的主要成分是铁,通常还含有2%-4.3%的杂质碳,请判断生铁属于_____(填“复合材料”、“合金”、“有机高分子材料”“硅酸盐材料”之一)。
(4)取5.8克生铁样品于烧杯中,加入10%硫酸溶液充分反应,生成气体与加入硫酸溶液的质量关系如下图所示,计算当加入硫酸溶液98g时,所得不饱和溶液中溶质的质量__________ (生铁中的杂质不与硫酸反应,也不溶于水)
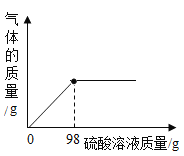
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某合金由铜与锌组成。现欲测定其组成,进行如下实验:取该合金样品30g放入烧杯中,然后将200g溶质质量分数为19.6%的稀硫酸平均分四份依次加入该烧杯中,每次均充分反应。实验数据如下:
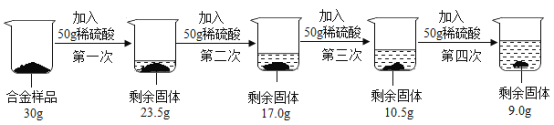
请计算:
(1)该合金中铜的质量为______________________g。
(2)第三次加入稀硫酸充分反应后,所得溶液中溶质的质量分数__________________(写出简明计算过程,结果保留一位小数)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知某固体混合物X中,可能含有CuSO4、NaCl、NH4NO3、FeCl3四种物质中的两种或多种。欲探究其组分,按如图所示进行探究实验,出现的现象如图中所述:(设过程中所有发生的反应都恰好完全进行)
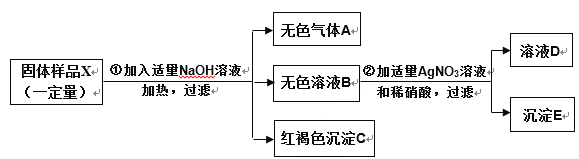
试根据上述实验信息,回答下列问题:
(1)将气体A通入无色酚酞试液,溶液呈_________色。
(2)沉淀C的化学式是________。
(3)固体样品X中,上述四种物质中,一定存在的物质是(写化学式)___________,一定不存在的物质是(写化学式)____________。
(4)实验证明,在溶液D中,肯定存在的酸根离子是(写离子符号)________________。
(5)写出步骤②中发生反应的一个化学方程式:______________。
(6)固体样品X中,仍不能确定的物质是(写化学式)___________,你的理由是________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】近日,我国企业成功研发圆珠笔笔头用新型不锈钢材料,标志着笔头用材料的国产化、自主化进程迈出了关键一步。笔头不锈钢材料中含有碳、铁、钨等元素。如图是其元素的部分信息。下列说法正确的是

A. 碳元素只能形成二种单质
B. 铁是地壳中含量最多的金属元素
C. 一个钨原子的质量为183.84g
D. 碳、铁、钨的原子核外电子数依次增加
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】73g10%的盐酸跟80g某浓度的氢氧化钠溶液恰好完全反应,将反应后的溶液蒸发掉108.8g水后,冷却到20℃时,溶液恰好达到饱和。请计算:
(1)原氢氧化钠溶液中溶质的质量________。
(2)原氢氧化钠溶液中溶质的质量分数_______。(结果保留到1%)
(3)20℃时,所得饱和溶液中溶质的质量分数_______。(结果保留到1%)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com