
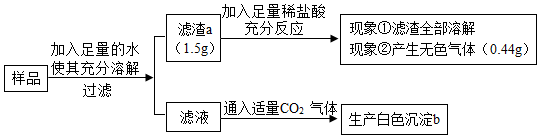
| A. | 滤渣a是CaCO3 | |
| B. | 白色沉淀b中可能含有MgCO3 | |
| C. | 滤液中一定存在的溶质是NaCl、BaCl2、NaOH | |
| D. | 该白色固体样品中一定含有CaCO3、BaCl2、NaOH、MgCl2,可能含有Na2SO4 |
分析 根据碳酸钙难溶于水,钡离子和硫酸根离子会生成硫酸钡沉淀,氢氧化钠和氯化镁反应会产生氢氧化镁沉淀,碳酸钙和盐酸反应会生成二氧化碳气体,结合化学方程式计算等知识进行分析.
解答 解:样品溶于水得到滤渣1.5g,能够全部溶于稀盐酸,且产生0.44g的二氧化碳,说明沉淀一定含有碳酸钙,一定没有硫酸钡,则一定无硫酸钠;
设产生0.44g的二氧化碳需要碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 0.44g
则$\frac{100}{44}=\frac{x}{0.44g}$,解得x=1g<1.5g,因此沉淀还有氢氧化镁;则沉淀a是碳酸钙和氢氧化镁;故A错误;
滤液通入二氧化碳产生沉淀,说明是二氧化碳和氢氧化钠反应产生碳酸钠,碳酸钠和氯化钡反应产生的碳酸钡沉淀,因此滤液中溶质的成分除氯化钠还有氢氧化钠和氯化钡;故C正确;
样品溶于水得到滤渣1.5g,能够全部溶于稀盐酸,且产生0.44g的二氧化碳,说明沉淀一定含有碳酸钙,一定没有硫酸钡,则一定无硫酸钠,故D错误;
故选:C.
点评 本题为框图式推断题,在解此类题时,首先分析题中所给物质的性质,然后依据题中的现象确定各种物质的存在性,最后确定混合物的成分.


科目:初中化学 来源: 题型:多选题
| 实验内容 | 实验结论 | |
| A | 燃着的木条置于一集气瓶瓶中,木条立即熄灭 | 气体一定是CO2或N2 |
| B | 二氧化硫气体通入紫色石蕊试液中,石蕊试液变红色 | 二氧化硫具有酸性 |
| C | 用玻璃棒分别蘸取酒精和水,放在酒精灯火焰上加热片刻 | 燃烧的条件之一是物质具有可燃性 |
| D | 氯化钡溶液滴入某溶液中,出现白色沉淀 | 溶液中可能含有CO32-或Ag+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 硝苯地平控释片是一种治疗高血压药物,其主要成份为硝苯地平(C17H18N2O6).请回答下列问题:
硝苯地平控释片是一种治疗高血压药物,其主要成份为硝苯地平(C17H18N2O6).请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 为测定某氮肥中硫酸铵的纯度(即质量分数)是否与如图标签相符,小林取一定量该氮肥样品与烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如表
为测定某氮肥中硫酸铵的纯度(即质量分数)是否与如图标签相符,小林取一定量该氮肥样品与烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如表| 反应前 | 反应后 | |
| 烧杯和样品溶液总质量 | 氯化钡溶液质量 | 过滤后烧杯和溶液总质量(滤液的损失忽略不计) |
| 45g | 55g | 76.7g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 千百年来,如皋人携手自然,铸就了独具魅力的三张名片:长江、长绿、长寿.
千百年来,如皋人携手自然,铸就了独具魅力的三张名片:长江、长绿、长寿.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com