
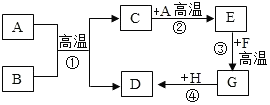
 A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种盐.它们的转化关系如图所示.请回答:
A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种盐.它们的转化关系如图所示.请回答:分析 根据题意,B为黑色固体,D为红色固体单质,则D为铜,B为氧化铜,结合碳与氧化铜在高温下反应生成铜和二氧化碳,则A为碳,C为二氧化碳;二氧化碳与碳在高温下反应生成一氧化碳,则E为一氧化碳;F为红色固体,结合氧化铁是一种红棕色固体,一氧化碳与氧化铁反应生成铁和二氧化碳;H溶液中的溶质是一种盐,铁与硫酸铜溶液反应生成硫酸亚铁溶液和铜;进行分析解答.
解答 解:B为黑色固体,D为红色固体单质,则D为铜,B为氧化铜,碳与氧化铜在高温下反应生成铜和二氧化碳,则A为碳,C为二氧化碳;二氧化碳与碳在高温下反应生成一氧化碳,则E为一氧化碳;F为红色固体,氧化铁是一种红棕色固体,一氧化碳与氧化铁反应生成铁和二氧化碳;H溶液中的溶质是一种盐,铁与硫酸铜溶液反应生成硫酸亚铁溶液和铜,则H为硫酸铜溶液,G为铁,带入验证符合转化关系,因此:
(1)B为氧化铜,E为一氧化碳;故填:CuO;CO;
(2)反应①是碳和氧化铜在高温的条件下反应生成铜和二氧化碳,反应②是二氧化碳与碳在高温下反应生成一氧化碳,属于化合反应;故答案为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;化合反应;
(3)反应④可以是铁和铜盐,如硫酸铜的反应,故反应的方程式为:Fe+CuSO4=FeSO4+Cu(合理即可).
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验方案或结论 |
| A | 除去铜粉中含有的少量铁粉 | 将混合固体加入到足量稀盐酸中,充分反应后过滤、洗涤、干燥 |
| B | 为了除去粗盐中的Ca2+、Mg2+、SO42-及泥砂,可将粗盐溶于水,然后进行下列五项操作①过滤;②加过量NaOH溶液; ③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液 | 操作顺序是:②④⑤①③ |
| C | 除去CaCl2溶液中的少量稀盐酸 | 加入过量的碳酸钙,过滤 |
| D | 鉴别NaCl溶液、Na2SO4溶液和(NH4)2SO4溶液 | 各取少量于试管中,分别滴加Ba(OH)2溶液,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 预期现象 | 结论 |
| 配方溶液中含有氢氧化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
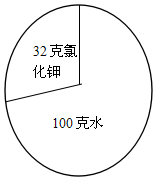
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验内容 | 实验现象 | 分析与判断 |
| 1盐和金属的反应 取一支洁净的试管,向试管中加入3ml的硫酸铜溶液,小心地加入一根用砂纸打磨光亮的铁丝,静置 | 铁丝表面生成红色固体,溶液由蓝色变浅绿色 | 化学方程式Fe+CuSO4=FeSO4+Cu |
| 2盐和碱的反应 取一支洁净的试管,向试管中加入约2ml碳酸钠溶液,用滴管向碳酸钠溶液中逐滴滴加氢氧化钙或氢氧化钡溶液,观察 | 生成白色沉淀 | 原因是生成的CaCO3或BaCO3(填化学式)难溶于水 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
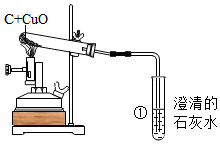 某同学为了探究木炭和氧化铜在高温条件下生成的气体产物的成分,提出了如下猜想:
某同学为了探究木炭和氧化铜在高温条件下生成的气体产物的成分,提出了如下猜想:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 水质主要成分(mg/L) | |
| 偏硅酸(H2SiO3) 28.9-42.9 碳酸氢根(HCO${\;}_{3}^{-}$) 173-205 氯离子(Cl-) 1.0-8.0 硫酸根(SO42-) 16.06-19.52 镁 2.5-7.5 | 锶(Sr) 0.01-0.32 钙 5-45 钠(Na+)45-70 钾(K+) 0.5-2.0 PH 7.8±0.5 |
 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com