



科目:初中化学 来源: 题型:
 如图是家用豆浆机,据图回答下列问题.
如图是家用豆浆机,据图回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验编号 | KClO3/g | 氧化物 | 产生气体的体积(mL) | 耗时(s) |
| 1 | 0.6 | 67 | 1 800 | |
| 2 | 0.6 | 0.2g 二氧化锰 | 67 | 36.5 |
| 3 | 0.6 | mg氧化铁 | 67 | 89.5 |
| 实验装置 | 实验现象 | 实现分析 |
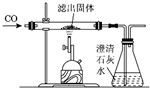 | 玻璃管中红色固体全部变黑 | 生成了铁 |
| 锥形瓶中石灰水变浑浊 | 产生二氧化碳 |
| 铁粉 | 氧化亚铁 | 氧化铁 | 四氧化三铁 | |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 磁性 | 有 | 无 | 无 | 有 |
| 与CO | 不反应 | 反应 | 反应 | 反应 |
| 与稀盐酸 | 反应生成氯化亚铁和水 | 生成氯化铁和水 | 生成氯化亚铁、氯化铁和水 | |
| 与硫酸铜溶液 | 反应 | 不反应 | 不反应 | 不反应 |
| 步骤 | 实验操作 | 实验现象 | 结论和解释 |
| 1 | 用磁铁吸引剩余固体 | 剩余固体中没有氧化亚铁. | |
| 2 | 向剩余固体中加入足量硫酸铜溶液 | 黑色固体全部变成红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:
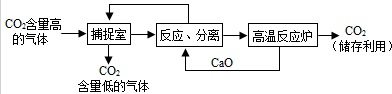
| A、高温反应炉中产生的CO2可不进行处理 |
| B、该方法可减少碳排放 |
| C、整个过程中,只有一种物质可以循环利用 |
| D、“反应分离”中,分离物质的基本操作是蒸发、结晶 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、用BaCl2溶液除去废水中的稀硫酸使其呈中性 |
| B、用稀硫酸和NaOH区分NH4NO3、KNO3和K2CO3 |
| C、用Ba(OH)2溶液区分MgCl2溶液和稀硫酸 |
| D、用稀硫酸与Fe2O3反应制取FeSO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 金属 | 空气 | 稀硫酸 | 硝酸银溶液 |
| 锌 | × | √ | √ |
| 铜 | × | × | √(A) |
| 镁 | √ | √ | √ |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com