
 =4g;则反应后固体的质量为:
=4g;则反应后固体的质量为: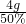 =8g,所以生成的二氧化碳质量是10g-8g=2g;
=8g,所以生成的二氧化碳质量是10g-8g=2g; CaO+CO2↑
CaO+CO2↑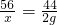
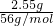 =0.05mol
=0.05mol

 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
| 实验步骤 | Ⅰ.将过量稀盐酸加入烧杯中并称重 | Ⅱ.称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 | Ⅲ.待反应完全后,称重 |
| 实验图示 |  | ||
| 实验数据 | 烧杯和稀盐酸的质量为100.0g | 石灰石样品的质量为15.0g | 烧杯和其中混合物的质量为110.6g |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2013年上海市闵行区中考化学一模试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com