
分析 【方案一】根据可燃物燃烧的条件进行分析解答;
【方案二】根据可燃物燃烧的条件进行分析解答;
【反思与评价】根据方案一和方案二的装置不同进行分析解答;
【拓展与应用】(1)根据化学反应前后原子的种类和数目不变进行分析解答;根据有机物的概念进行分析解答;
(2)根据反应物的状态和反应条件进行分析判断;根据影响化学反应速度的因素进行分析解答.
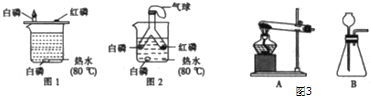
解答 解:【方案一】由图1比较铜片上的白磷和红磷,白磷能燃烧而红磷不能燃烧,说明燃烧温度要达到可燃物的着火点;比较铜片上的白磷和水中的白磷,铜片上的白磷能燃烧而水中的白磷不燃烧,说明燃烧需要有氧气参加;要使水中的白磷发生燃烧,可以向水中白磷处通入氧气可空气;故填:铜片上的白磷燃烧而水中的白磷没有燃烧;用导管对着水中白磷通氧气或空气;
【方案二】由图2将装有白磷和红磷的Y型管放入热水中的目的是探究可燃物燃烧温度需达到可燃物的着火点;故填:探究可燃物燃烧温度需达到可燃物的着火点;
【反思与评价】比较图1和图2可知二者的最大区别是,图2装置是密闭的产生的五氧化二磷不能排放到空气中,五氧化二磷是有害物质,故图2装置比图1装置更环保,故填:环保;
【拓展与应用】(1)根据化学反应前后原子的种类和数目不变,反应物中原子个数如下:Ca原子1个;C原子2个;H原子4个;O原子2个,生成物中已知物质中含有的原子个数如下:C原子2个;H原子2个;由此可知R中含有1个Ca原子;2个H原子;2个O原子,故R的化学式为:Ca(OH)2,有机物是指含碳的化合物,但不包括一氧化碳、二氧化碳、碳酸钙等物质,根据题中化合物C2H2的化学式可知该物质属于有机物;故填:Ca(OH)2;有机物;
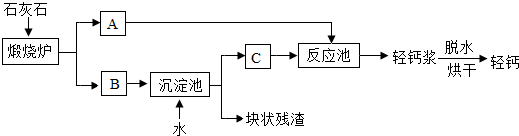
(2)由制取C2H2用的是固态的电石和液态的水反应不需要加热,故需要选用B装置作为发生装置;电石与水反应剧烈,为控制好其反应速率,常用饱和食盐水代替水,饱和食盐水中的氯化钠降低了溶液中水的浓度从而降低了反应速率而且反应过程中会有部分氯化钠结晶析出,覆盖在电石表面阻碍水与电石的接触,从而也降低了反应速率;从反应装置上来讲也可以通过控制加入水的速率来达到控制反应速率的方法,通常情况下是将长颈漏斗换成分液漏斗或注射器来控制水的加入速率;故填:饱和食盐水中的氯化钠降低了水的浓度或有部分氯化钠会析出,覆盖在电石表面,使电石与水的接触面积减小,从而降低反应速率;分液漏斗或注射器代替长颈漏斗控制加水的速率.
点评 此题考查可燃物燃烧条件的探究和气体制备的知识,其中对控制反应速率的探究是本题的难点,掌握影响化学反应速率的因素知识是突破难点的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 组成石墨和金刚石的原子相同,而金刚石硬度很大,所以石墨的硬度也很大 | |
| B. | 力的作用是相互的,所以晓铭推墙的力的大小一定等于他所受的重力 | |
| C. | 碱溶液中含有氢元素,所以含有氢元素的就是碱 | |
| D. | 水和冰的化学式相同,所以组成水和冰的分子是同一种分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
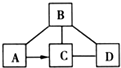 已知A-D是初中化学的常见物质.A和D是两种常见的碱;B是一种常见的酸,且只含有两种元素;C是一种钠盐.它们相互间转化或发生反应的关系如图所示.(“-”表示两种物质间能发生化学反应,“→”表示两种物质间的转化关系.)
已知A-D是初中化学的常见物质.A和D是两种常见的碱;B是一种常见的酸,且只含有两种元素;C是一种钠盐.它们相互间转化或发生反应的关系如图所示.(“-”表示两种物质间能发生化学反应,“→”表示两种物质间的转化关系.)查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 测量项目 | 实验前 | 实验后 | |
| 烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
| 体积/mL | 80.0 | 54.5 | 126.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
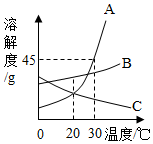 如图是A、B、C三种物质的溶解度曲线,请你根据此图完成下列问题:
如图是A、B、C三种物质的溶解度曲线,请你根据此图完成下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com