

 2CO;
2CO;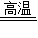 2Fe+3CO2;
2Fe+3CO2;

科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象 | 结论 |
| ①取少量样品于试管中并加入过量的稀HNO3 | 有气泡 有气泡 |
存在Na2CO3 存在Na2CO3 |
| ②再向实验①的溶液中加入AgNO3溶液 | 白色沉淀 白色沉淀 |
含有NaCl 含有NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:
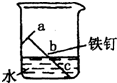 (2006?咸宁)据统计世界上每年因生锈损失的钢铁约占年产量的四分一,刘星同学为探究铁的锈蚀条件,设计了如图所示的装置,在一个小烧杯中放入一铁钉,使其一半置于水面以下,一半置于空气中.请回答:
(2006?咸宁)据统计世界上每年因生锈损失的钢铁约占年产量的四分一,刘星同学为探究铁的锈蚀条件,设计了如图所示的装置,在一个小烧杯中放入一铁钉,使其一半置于水面以下,一半置于空气中.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:022
(
南通,2006)双氧水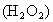 既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.
既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.
(1)
小明从试剂商店购得一瓶质量分数为30%的双氧水,用于制取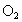 .若配制5%的双氧水600g,需30%的双氧水的质量为________;
.若配制5%的双氧水600g,需30%的双氧水的质量为________;
(2)
为了操作方便,改称量液体的质量为量取液体的体积.若配制5%的双氧水,应取30%的双氧水(密度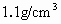 )与水的体积比为________.
)与水的体积比为________.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com