
【题目】闪锌矿(主要成分为ZnS)经熔烧得锌焙砂,锌焙砂主要含ZnO、ZnFe3O4,以及少量FeO、CuO,工业上用其制备金属锌,具体过程如图所示。
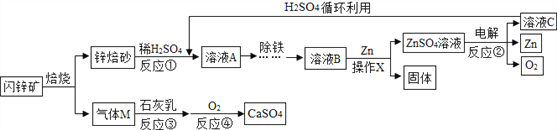
(1)操作X的名称是_______,需要使用的玻璃仪器有 _______ 、烧杯、玻璃棒。
(2)进行反应①时,要将锌焙砂粉碎成细小颗粒,目的是_______________。
(3)ZnFe2O4可看作两种氧化物的结合,与稀H2SO4反应生产两种盐,分别是ZnSO4和______(填化学式)。
(4)写出反应②的化学方程式:___________。
(5)反应③的气体M是:___(填化学式)。
【答案】 过滤 漏斗 增大反应物的接触面积,使反应更加充分快速 Fe2(SO4)3 2ZnSO4+2H2O=== 2H2SO4+2Zn+O2↑ SO2
【解析】(1)操作X将固体和液体分离,故是过滤;过滤需要使用的玻璃仪器有漏斗 、烧杯、玻璃棒。
(2)进行反应①时,要将锌焙砂粉碎成细小颗粒,目的是增大反应物的接触面积,使反应更加充分快速;
(3)ZnFe2O4中铁元素的化合价为+3价,所以与稀硫酸反应后生成Fe2(SO4)3 ;
(4)反应②硫酸锌和水在通电的条件下反应生成锌、氧气和硫酸,反应方程式为2ZnSO4+2H2O=== 2H2SO4+2Zn+O2↑;
(5)ZnS焙烧后生成的气体是SO2


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案科目:初中化学 来源: 题型:
【题目】化学兴趣小组设计了如图所示的微型实验。
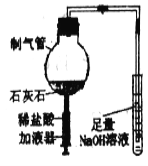
(1)在制气管中加入石灰石,推压加液器活塞加入适量稀盐酸,请用化学方程式表示其反应原理。
(2)当制气管中的反应停止后,试管中溶液倒吸进制气管中,产生白色沉淀,请解释产生上述现象可能的原因。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】镁在航空航天领域有广泛应用,刚刚首飞的C919客机上大量应用了含镁材料。镁元素的相关信息如图所示。请回答下列问题:
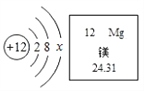
(1)镁原子的质子数为________,x=_____________。
(2)镁属于____________元素(填“金属”或“非金属”),金属镁在化学反应在容易__________(填写“得到”或“失去”)电子。
(3)海水中含有丰富的氯化镁,目前工业上绝大多数的金属镁是从海水中提取的,其生产流程如图:
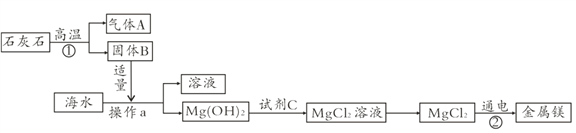
在上述流程中,操作a的名称是____,反应②的化学方程式为________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
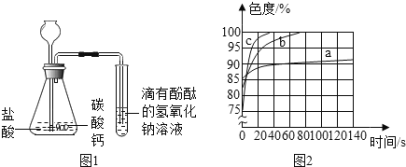
【题目】(9分)某研究性学习小组在验证“碱使酚酞试液变红”的实验时,发现一个意外现象:将酚酞试液滴入某NaOH溶液中,溶液变成了红色,可是过一会儿红色却消失。
【提出问题】是什么原因导致滴有酚酞的NaOH溶液由红色褪为无色?
【猜想与假设】他们分别对这种意外现象作如下猜想:
甲同学:可能是酚酞与O2发生了反应;
乙同学:可能是NaOH溶液与空气中的CO2发生了反应;
丙同学:可能与 大小有关;
【设计实验】三位同学分别设计实验验证自己的猜想:
(1)甲同学设计了如下实验,请你填写下表。
实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
①将NaOH溶液加热煮沸 | ① | 溶液变红,过一会儿红色消失 | 甲同学猜想___________(填“正确”或不正确”)新课 |
②向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方 | ② |
(2)乙同学设计如图一装置进行实验,一段时间后,试管中溶液的红色褪去,于是认定自己的猜想正确。写出CO2与NaOH溶液反应的化学方程式: 。
甲同学认为乙同学的实验不够严谨,理由是: 。
(3)丙同学使用了色度传感器测溶液的颜色。他在a、b、c三个比色皿中分别加入等量5%、10%、20%的NaOH溶液,然后各滴加2滴酚酞试液。溶液颜色的变化曲线如图[说明:溶液无色时色度值(透过率)为100%]。请你观察图二写出规律性结论:_____________________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种物质的溶解度曲线,下列说法不正确的是( )

A. P点表示t1℃时,a、c两种物质的溶解度相等
B. 将c的饱和溶液变为不饱和溶液,可采用降温的方法
C. t2℃时,将30g a物质加入到50g水中充分搅拌,得到75g a的饱和溶液
D. 将t1℃时a、b、c三种物质的饱和溶液升温至t2℃,其溶质质量分数由大到小的顺序是a>b>c
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A﹣H均为初中化学常见的物质,其中A、C常温下是气体,且组成元素相同,C的固体俗名叫“干冰”,B是赤铁矿的主要成分,E能用于改良酸洗土壤,H是紫红色金属。他们的相互转化关系如图(图中反应条件均已略去):
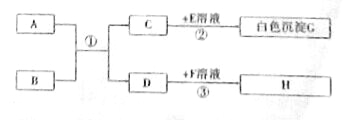
请回答下列问题:
(1)写出E物质的化学式 。
(2)写出反应①的化学方程式 。
(3)反应③的基本反应类型是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~G是初中化学常见的物质,B和D能参与光合作用,F可用于改良酸性土壤. 它们之间的关系如图所示(“﹣”表示相连两物质之间能发生反应,“→”表示由某一物成转化为另一物质,部分反应物、生成物及反应条件已略去),每个虚线圈中各反应的基本反应类型相同.
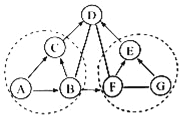
(1)写出物质的化学式:A_______,G__________.
(2)反应F→E的基木反应类型是__________.
(3)反应D﹣F的化学方程式是__________________.
(4)反应G→E的现象是________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸铜是一种应用极其广泛的化工原料,易溶于水而不易溶于酒精;铜离子完全沉淀的pH是5左右,铁离子完全沉淀的pH是2左右。以下是某工厂用含铁废铜为原料生产胆矾(CuSO4·5H2O)和副产物石膏(CaSO4·2H2O)的生产流程示意图:

胆矾和石膏在不同温度下的溶解度(g/100g水)如表。
温度(℃) | 20 | 40 | 60 | 80 | 100 |
石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
请回答下列问题:
(1)红褐色滤渣的主要成分是____________;
(2)铜和稀硝酸反应的化学方程式3Cu+8HNO3=_____________+2NO↑+4H2O;
(3)石灰浆调pH大约要调节到___________
A. 2 B. 5 C. 7 D. 10
(4)操作I最后温度应该控制在___________℃左右;
(5)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、_______、过滤、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是__________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题:

(1)在第三周期中,各原子结构的共同之处是 ;该周期中,各原子核外电子排布的变化规律是 .
(2)在第三周期中,元素类型的变化情况是:从左到右由 元素过渡到 元素,并以 元素结尾.
(3)写出核外电子排布与氖原子相同的阳离子和阴离子符号各一个:
阳离子 ;阴离子 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com