
”¾ĢāÄæ”æŌĶĮĻĀĆęŠÅĻ¢²ÄĮĻ£¬²¢»Ų“šĻą¹ŲĪŹĢā£ŗ
ĀČĘų£¬»ÆѧŹ½ĪŖ![]() ”£³£ĪĀ³£Ń¹ĻĀĪŖ»ĘĀĢÉ«”¢ÓŠĒæĮŅ“Ģ¼¤ŠŌĘųĪ¶µÄÓŠ¶¾ĘųĢ壬ĆܶȱČæÕĘų“ó£¬æÉČÜÓŚĖ®£¬Ņ×Ń¹Ėõ£¬æÉŅŗ»ÆĪŖ½š»ĘÉ«ŅŗĢ¬·Õ”£ĀČĘųÖŠ»ģŗĶĢå»ż·ÖŹżĪŖ5%ŅŌÉĻµÄĒāĘųŹ±£¬ÓöĒæ¹ā»į·¢Éś¾ēĮŅµÄ»Æѧ·“Ӧɜ³ÉĀČ»ÆĒāĘųĢ壬·Å³öµÄČČĮæŹ¹ĘųĢå¼±¾ēÅņÕĶ£¬æÉÄÜŌģ³É±¬ÕصÄĪ£ĻÕ£»½šŹōÄĘŌŚĀČĘųĄļæÉŅŌ¾ēĮŅČ¼ÉÕ£¬²śÉś“óĮæµÄ°×ŃĢ£¬Ķ¬Ź±·Å³öČČĮ攣ĀČĘųŌŚŌēĘŚ³£×÷ĪŖŌģÖ½”¢·ÄÖƹ¤ŅµµÄĘÆ°×¼Į£»ĮķĶāĀČĘųĶØČėĖ®ÖŠ£¬»įÉś³É
”£³£ĪĀ³£Ń¹ĻĀĪŖ»ĘĀĢÉ«”¢ÓŠĒæĮŅ“Ģ¼¤ŠŌĘųĪ¶µÄÓŠ¶¾ĘųĢ壬ĆܶȱČæÕĘų“ó£¬æÉČÜÓŚĖ®£¬Ņ×Ń¹Ėõ£¬æÉŅŗ»ÆĪŖ½š»ĘÉ«ŅŗĢ¬·Õ”£ĀČĘųÖŠ»ģŗĶĢå»ż·ÖŹżĪŖ5%ŅŌÉĻµÄĒāĘųŹ±£¬ÓöĒæ¹ā»į·¢Éś¾ēĮŅµÄ»Æѧ·“Ӧɜ³ÉĀČ»ÆĒāĘųĢ壬·Å³öµÄČČĮæŹ¹ĘųĢå¼±¾ēÅņÕĶ£¬æÉÄÜŌģ³É±¬ÕصÄĪ£ĻÕ£»½šŹōÄĘŌŚĀČĘųĄļæÉŅŌ¾ēĮŅČ¼ÉÕ£¬²śÉś“óĮæµÄ°×ŃĢ£¬Ķ¬Ź±·Å³öČČĮ攣ĀČĘųŌŚŌēĘŚ³£×÷ĪŖŌģÖ½”¢·ÄÖƹ¤ŅµµÄĘÆ°×¼Į£»ĮķĶāĀČĘųĶØČėĖ®ÖŠ£¬»įÉś³É![]() ŗĶ
ŗĶ![]() £Ø“ĪĀČĖį£©£¬“ĪĀČĖį¾ßÓŠĻū¶¾É±¾śµÄ×÷ÓĆ£¬ĖłŅŌĀČĘųŅ²³£ÓĆÓŚ×ŌĄ“Ė®Ļū¶¾”£
£Ø“ĪĀČĖį£©£¬“ĪĀČĖį¾ßÓŠĻū¶¾É±¾śµÄ×÷ÓĆ£¬ĖłŅŌĀČĘųŅ²³£ÓĆÓŚ×ŌĄ“Ė®Ļū¶¾”£
£Ø1£©ĀČĘųµÄÖ÷ŅŖĪļĄķŠŌÖŹÓŠ_________________”£
£Ø2£©ÄĘŌŚĀČĘųĄļ¾ēĮŅČ¼ÉÕ£¬²śÉśµÄ”°°×ŃĢ”±ŹĒ________________”£
£Ø3£©![]() £Ø“ĪĀČĖį£©ÖŠĀČŌŖĖŲµÄ»ÆŗĻ¼ŪŹĒ________________”£
£Ø“ĪĀČĖį£©ÖŠĀČŌŖĖŲµÄ»ÆŗĻ¼ŪŹĒ________________”£
£Ø4£©ĀČĘųŗĶĒāĘų·“Ó¦µÄĪÄ×Ö±ķ“ļŹ½ĪŖ£ŗ_________________”£
”¾“š°ø”æ³£ĪĀ³£Ń¹ĻĀĪŖ»ĘĀĢÉ«”¢ÓŠĒæĮŅ“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢ壬ĆܶȱČæÕĘų“ó£¬æÉČÜÓŚĖ®£¬Ņ×Ń¹Ėõ£¬æÉŅŗ»ÆĪŖ½š»ĘÉ«ŅŗĢ¬ĀČ ĀČ»ÆÄĘ¹ĢĢ劔æÅĮ£ ![]()
![]()
”¾½āĪö”æ
£Ø1£©ĀČĘųµÄÖ÷ŅŖĪļĄķŠŌÖŹÓŠ£ŗ³£ĪĀ³£Ń¹ĻĀĪŖ»ĘĀĢÉ«”¢ÓŠĒæĮŅ“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢ壬ĆܶȱČæÕĘų“ó£¬æÉČÜÓŚĖ®£¬Ņ×Ń¹Ėõ£¬æÉŅŗ»ÆĪŖ½š»ĘÉ«ŅŗĢ¬ĀČ£»
£Ø2£©ÄĘŌŚĀČĘųĄļ¾ēĮŅČ¼Éյķ“Ó¦ŌĄķ£ŗ2Na£«Cl2![]() 2NaCl£¬²śÉśµÄ”°°×ŃĢ”±ŹĒ£ŗĀČ»ÆÄĘ¹ĢĢ劔æÅĮ£;
2NaCl£¬²śÉśµÄ”°°×ŃĢ”±ŹĒ£ŗĀČ»ÆÄĘ¹ĢĢ劔æÅĮ£;
£Ø3£©![]() £Ø“ĪĀČĖį£©ÖŠ£¬ĒāŌŖĖŲĻŌ+1¼Ū£¬ŃõŌŖĖŲĻŌ-2¼Ū£¬ÉčĀČŌŖĖŲ»ÆŗĻ¼ŪĪŖx£¬ŌņÓŠ£ŗ£Ø+1£©+x+£Ø-2£©=0£¬Ōņx=+1£¬ĀČŌŖĖŲµÄ»ÆŗĻ¼ŪŹĒ£ŗ+1¼Ū£»
£Ø“ĪĀČĖį£©ÖŠ£¬ĒāŌŖĖŲĻŌ+1¼Ū£¬ŃõŌŖĖŲĻŌ-2¼Ū£¬ÉčĀČŌŖĖŲ»ÆŗĻ¼ŪĪŖx£¬ŌņÓŠ£ŗ£Ø+1£©+x+£Ø-2£©=0£¬Ōņx=+1£¬ĀČŌŖĖŲµÄ»ÆŗĻ¼ŪŹĒ£ŗ+1¼Ū£»
£Ø4£©ĀČĘųŗĶĒāĘų·“Ӧɜ³ÉĀČ»ÆĒā£¬·“Ó¦µÄĪÄ×Ö±ķ“ļŹ½ĪŖ£ŗĒāĘų+ĀČĘų![]() ĀČ»ÆĒā”£
ĀČ»ÆĒā”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
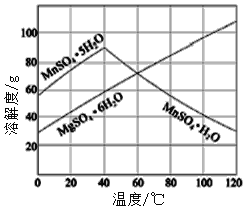
”¾ĢāÄæ”æÖŹĮæĻąµČµÄĮ½øöÉձ֊װČėµČÖŹĮæµÄŠæ·ŪŗĶĢś·Ū£¬ŌŁ·Ö±š·ÅČėÖŹĮæĻąµČ”¢ČÜÖŹÖŹĮæ·ÖŹżĻąĶ¬µÄĻ”ĮņĖįÖŠ£¬Éś³ÉĒāĘųÖŹĮæ(m)Ėę·“Ó¦Ź±¼ä(t)µÄ±ä»ÆĒśĻßČē19ĢāĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·Ø“ķĪóµÄÓŠ( )
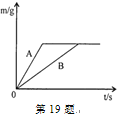
¢ŁA±ķŹ¾ŠæŗĶĻ”ĮņĖįµÄ·“Ó¦ĒśĻß
¢Ś·“Ó¦½įŹųŗóĮ½ÖÖ½šŹōŅ»¶Ø¶¼ÓŠŹ£Óą
¢ŪĮ½·ŻČÜŅŗÖŠµÄĮņĖįŅ»¶Ø¶¼·“Ó¦Ķź
¢Ü·“Ó¦µōµÄŠæŗĶĢśµÄÖŹĮæ±ČĪŖ56:65
¢Ż·“Ó¦½įŹųŗóĻūŗÄĮ½ÖÖ½šŹōµÄÖŹĮæĻąµČ
¢Ž·“Ó¦½įŹųŗóĮ½ÉÕ±ÖŠĪļÖŹµÄÖŹĮæĻąµČ
A.2øöB.3øöC.4øöD.5øö
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŖĖŲÖÜĘŚ±ķŹĒѧĻ°»ÆѧµÄÖŲŅŖ¹¤¾ß”£ĻĀ±ķĪŖŌŖĖŲÖÜĘŚ±ķÖŠ²æ·ÖŌŖĖŲµÄĻą¹ŲŠÅĻ¢£¬ĒėĄūÓĆĻĀ±ķ»Ų“šĻą¹ŲĪŹĢā£ŗ
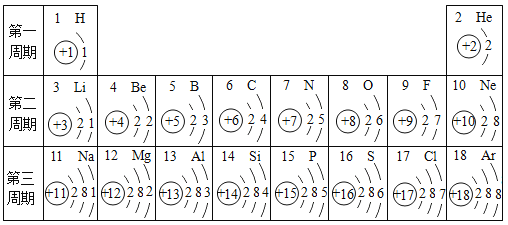
£Ø1£©ĮņŌŖĖŲµÄŌ×ÓŠņŹżŹĒ___________£¬ĖüŹōÓŚ_________£ØĢī”°½šŹō”±³É”°·Ē½šŹō”±£©ŌŖĖŲ£¬±ķÖŠÄŹŌŖĖŲĪ»ÓŚŌŖĖŲÖÜĘŚ±ķÖŠµÄµŚ_______ÖÜĘŚ”£
£Ø2£©ÓėŌŖĖŲµÄ»ÆѧŠŌÖŹ¹ŲĻµ×īĆÜĒŠµÄŹĒŌ×ÓµÄ________£»¾ö¶ØŌŖĖŲÖŹĮæµÄŹĒŌ×ÓµÄ________£»¹čŌŖĖŲŗĶŃõŌŖĖŲ²»Ķ¬ŌŅņŹĒ______________”£
£Ø3£©µŚČżÖÜĘŚŗĖĶāµē×ÓÅŲ¼µÄ¹ęĀÉŹĒ___________”£
£Ø4£©Š“³öŗĖĶāµē×ÓÅŲ¼ÓėÄŹŌ×ÓĻąĶ¬µÄŃōĄė×Ó·ūŗÅŹĒ__________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æMnSO4H2OŌŚ¹¤Ņµ”¢Å©ŅµµČ·½ĆęÓŠ¹ć·ŗµÄÓ¦ÓĆ”£
£ØŅ»£©Öʱø£ŗ¹¤ŅµÉĻÓĆ»Æ¹¤³§Ī²ĘųÖŠµĶÅضČSO2ÓėČķĆĢæó£ØÖ÷ŅŖ³É·ÖMnO2£¬ŌÓÖŹ½šŹōŌŖĖŲMg”¢Al”¢FeµČ£©ÖʱøMnSO4H2O¹ż³ĢČēĻĀ£ŗ
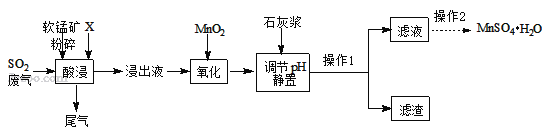
ŅŃÖŖ£ŗ½ž³öŅŗÖŠŃōĄė×ÓÖ÷ŅŖÓŠH+”¢Mn2+”¢Mg2+”¢Fe2+”¢Al3+µČ£»½ž³ö¹ż³ĢÖŠ·¢ÉśµÄÖ÷ŅŖ·“Ó¦»Æѧ·½³ĢŹ½ĪŖ£ŗMnO2+SO2=MnSO4”£
£Ø1£©Éś²śÖŠ½«ČķĆĢæó·ŪĖéµÄÄæµÄŹĒ____”£
£Ø2£©ĪļÖŹX×īŗĆŃ”ÓĆ_____”£
a.ŃĪĖį b.ĮņĖį c.ĻõĖį
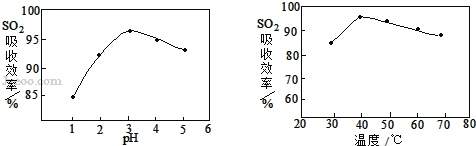
£Ø3£©Ėį½žŹ±SO2µÄĪüŹÕŠ§ĀŹÓėpH”¢ĪĀ¶ČµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾£¬ĪŖĢįøßSO2µÄĪüŹÕŠ§ĀŹ£¬Ėį½žŹ±pHæŲÖĘŌŚ____×óÓŅ£¬ĪĀ¶ČæŲÖĘŌŚ_________”ę×óÓŅ×īŹŹŅĖ”£
£Ø4£©Į÷³ĢÖŠ”°Ńõ»Æ”±²½ÖčµÄÄæµÄŹĒ½«Fe2+ Ńõ»ÆĪŖFe3+£¬ĒėĶźÉĘ·“Ó¦µÄ»Æѧ·½³ĢŹ½MnO2+2FeSO4+_______ = MnSO4 + Fe2(SO4)3 + 2H2O”””£
£Ø5£©¼ÓČėŹÆ»Ņ½¬µ÷½ŚpH£¬æɽ«Ńõ»ÆŗóµÄ½ž³öŅŗÖŠŌÓÖŹĄė×ÓŠĪ³ÉĒāŃõ»ÆĪļ³żČ„”£
ŅŃÖŖ£ŗ£ØŅ»£©ÓŠ¹ŲĒāŃõ»ÆĪļ³ĮµķpH¶ŌÓ¦±ķ
ĒāŃõ»ÆĪļ | Fe(OH)3 | Al(OH)3 | Mn(OH)2 | Mg(OH)2 |
æŖŹ¼³ĮµķpH | 1.8 | 4.1 | 8.3 | 9.4 |
ĶźČ«³ĮµķpH | 3.2 | 5.0 | 9.8 | 12.4 |
£Ø¶ž£©Fe3+ÄÜÓėKSCNČÜŅŗ×÷ÓĆĻŌŃŖŗģÉ«Ōņ¼ÓŹÆ»Ņ½¬Ź±Ó¦æŲÖĘČÜŅŗµÄpH·¶Ī§ĪŖ_________”£²ā¶ØČÜŅŗµÄpH×īŗĆŃ”____£Øa.pHŹŌÖ½ b.pH¼Ę£©£¬¼ģŃéFe3+ŹĒ·ń³ż¾”µÄ×ī¼Ń·½·ØŹĒ________”£
£Ø6£©²Ł×÷1°üĄØ¹żĀĖŗĶĻ“µÓ£¬¹żĀĖÓƵ½µÄ²£Į§ŅĒĘ÷ÓŠÉÕ±”¢²£Į§°ōŗĶ_____£¬Ļ“µÓµÄÄæµÄŹĒ________
£Ø7£©ŅŃÖŖĮņĖįĆĢ”¢ĮņĖįĆ¾½į¾§Ė®ŗĻĪļµÄČܽā¶ČĒśĻßČēĶ¼£¬Ōņ²Ł×÷2°üĄØ£ŗÕō·¢ÅØĖõ£¬___________£¬¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ”£
£Ø¶ž£©Ó¦ÓĆ£ŗ
£Ø8£©ÓĆMnSO4æɲā¶ØĖ®ÖŠČܽāŃõ”£·½·ØŹĒ£ŗČ”100mL Ė®Ńł£¬ŃøĖŁ¼ÓČė×ćĮæMnSO4ČÜŅŗ¼°ŗ¬ÓŠNaOHµÄKIČÜŅŗ£¬Į¢¼“ČūÉĻČū×Ó”¢Õńµ“£¬Ź¹Ö®³ä·Ö·“Ó¦£»“ņæŖČū×Ó£¬ŃøĖŁ¼ÓČėŹŹĮæµÄĻ”ĮņĖį£¬“ĖŹ±ÓŠI2Éś³É£»ŌŁÓĆ0.79gL©1Na2S2O3ČÜŅŗŗĶI2·“Ó¦£¬µ±ĻūŗÄNa2S2O3ČÜŅŗ 12.0mLŹ±·“Ó¦ĶźČ«”£ÓŠ¹Ų»Æѧ·“Ó¦·½³ĢŹ½ĻĀ£ŗ
¢Ł2MnSO4+O2+4NaOH=2MnO(OH)2+2Na2SO4£»
¢ŚMnO(OH)2 + 2KI + 2H2SO4 = MnSO4 + K2SO4 + I2 + 3H2O£»
¢ŪI2 + 2Na2S2O3 = Na2S4O6 + 2NaI”£
¼ĘĖćĖ®ŃłÖŠČܽāŃõµÄÅØ¶Č£ØŅŌmgL-1ĪŖµ„Ī»£©£¬Š“³ö¼ĘĖć¹ż³Ģ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧŠĖȤŠ”×éŃ”ŌńČ¼ÉÕĆ¾“ų½ųŠŠ¶ØĮæŹµŃéŃŠ¾æ
£Ø׏ĮĻ£©Ć¾³żĮĖÓėæÕĘųÖŠµÄŃõĘų·“Ó¦Ķā£¬»¹æÉŅŌÓėæÕĘųÖŠµÄµŖĘųŌŚµćČ¼Ģõ¼žĻĀÉś³É¹ĢĢåµŖ»ÆĆ¾Mg3N2£¬µŚŅ»×éĶ¬Ń§³ĘĮæĮĖ0.2gĆ¾“ų£¬ŌŚæÕĘųÖŠµćČ¼£¬ĶźČ«Č¼ÉÕŗ󣬳ĘĮæĖłµĆ¹ĢĢåÖŹĮæĪŖ0.30g”£µŚ¶žŠ”×éĶ¬Ń§¾õµĆµŚŅ»Š”×éµÄŹµŃ鏿¾Ż²»ŗĻĄķ£¬·ÖĪöŌŅņ²¢Éč¼ĘĮĖČēĻĀĶ¼ĖłŹ¾µÄŹµŃ飬ŹµŃé²½ÖčČēĻĀ£ŗ
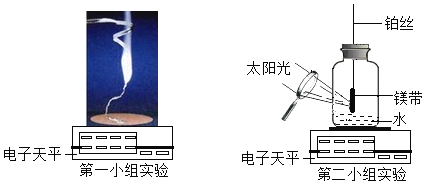
²½ÖčŅ»£ŗ½«0.24g“ņÄ„¹āĮĮµÄĆ¾“ų¹Ģ¶ØŌŚ“©¹żĘæČūµÄ²¬ĖæÉĻ(²¬Ėæ²»·“Ó¦)£¬¹ćæŚĘæŹ¢ĀśŃõĘų²¢Čū½ōĘæČū(ČēĶ¼ĖłŹ¾)£¬Ęæµ×ĮōÓŠŹŹĮæµÄĖ®£»
²½Ö趞£ŗÓŠ¾Ū¹ā¾µŅżČ¼Ć¾“ų£¬“żĘäĶźČ«Č¼ÉÕŗ󣬳ä·ÖÕšµ“ĘæÄŚµÄĖ®ŌŁ¾²ÖĆ£¬ĘæÄŚ°×ŃĢĶźČ«ĻūŹ§£¬ÓŠ°×É«¹ĢĢå³ĮµķŌŚĘæµ×£»(“ĖĢõ¼žĻĀŃõ»ÆĆ¾ÄŃČÜÓŚĖ®ĒŅ²»ÓėĖ®·“Ó¦)
²½ÖčČż£ŗ½«ĘæÄŚČ«²æµÄ¹ĢŅŗ»ģŗĻĪļ¹żĀĖ£¬øÉŌļĀĖÖ½¼°Ęä±ķĆęµÄĀĖŌüŗóŅ»Ęš³ĘĮ棬×ÜÖŹĮæĪŖ0.75g.(¹ĢĢåĖšŹ§ŗöĀŌ²»¼Ę)
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)Š“³öĆ¾“ųŌŚæÕĘųÖŠČ¼ÉյĻÆѧ·½³ĢŹ½(Ö»Š“Ņ»øö)_______
(2)¹ŲÓŚĮ½øöŠ”×鏵ŃéµÄĖµ·ØÕżČ·µÄŹĒ_____
A µŚŅ»×鏵Ń鏿¾Ż²»ŗĻĄķŹĒŅņĪŖ0.3g>0.24g£¬²»×ńŹŲÖŹĮæ¶ØĀÉ
B µŚ¶ž×鏵ŃéÖŠµÄĖ®¼ČæÉŅŌ¼ÓĖŁ×°ÖĆĄäČ“£¬ÓÖæÉŅŌĶعżĖ®°ļÖśŹÕ¼ÆĘæÄŚµÄÉś³ÉĪļ
C Ć¾“ųČ¼ÉÕŹ±ÓŠ°×ŃĢĘ®É¢µÄĻÖĻóĖµĆ÷·Ö×ÓŹĒÓĄ²»Ķ£ŠŖµÄ×÷ĪŽ¹ęŌņŌĖ¶ÆµÄ
D ĶعżµŚŅ»×鏵Ń鏿¾ŻæÉŅŌĶĘ²ā£¬Ć¾ŌŚæÕĘųÖŠČ¼ÉÕŅ»¶ØÉś³ÉĮĖµŖ»ÆĆ¾
E µŚ¶žŠ”×éĶ¬Ń§Ö»Šč³ĘĮæĆ¾“ųČ¼ÉÕĒ°ŗó·ā±ÕµÄ¹ćæŚĘæĢåĻµµÄ×ÜÖŹĮ棬¼“æÉŃéÖ¤ÖŹĮæŹŲŗć¶ØĀɶØĀÉ
(3)µŚ¶žŠ”×éĶ¬Ń§ŌŚ½ųŠŠŹµŃ鏱£¬ČōĪ““ņÄ„Č„³żĆ¾“ų±ķĆęµÄŃõ»ÆĤ£¬×īŗóĖūĆĒ³ĘĮæµÄĀĖÖ½ŗĶĀĖŌü×ÜÖŹĮæ»į____0.75g(Ģī> < =)
(4)øł¾ŻµŚ¶žŠ”×éĶ¬Ń§µÄŹµŃ鏿¾Ż£¬ČōŅŖµĆµ½ÓėŃõĘų·“Ó¦µÄÖŹĮ棬»¹±ŲŠė²āĮæ___ČōŹµŃé½į¹ūÓėÖŹĮæŹŲŗćĻņĪĒŗĻ£¬ĒėĶĘ²āŅŌÉĻ²āĮæÖµĪŖ_____
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆ»ÆѧÓĆÓļĢīæÕ£ŗ2øö¶žŃõ»ÆĢ¼·Ö×Ó________£»3øöĮņĖįøłĄė×Ó________£»ĀČ»ÆĆ¾ÖŠĆ¾ŌŖĖŲ»ÆŗĻ¼ŪĪŖ+2¼Ū________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻĻĀĮŠ×°ÖĆĶ¼»Ų“š¼ņĢā
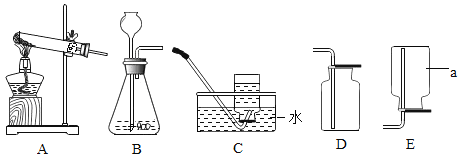
£Ø1£©Š“³öŅĒĘ÷aµÄĆū³Ę£ŗ______________”£
£Ø2£©ŹµŃéŹŅÓĆ¼ÓČČøßĆĢĖį¼ŲµÄ·½·ØÖĘČ”²¢ŹÕ¼ÆŃõĘų£¬Ó¦Ń”ÓƵķ¢Éś×°ÖĆĪŖ___________£ØĢīŠņŗÅ£¬ĻĀĶ¬£©£¬ČōŅŖŹÕ¼Æ½Ļ“æ¾»µÄŃõĘų£¬ŌņŹÕ¼Æ×°ÖĆĪŖ______________”£
£Ø3£©ŹµŃéŹŅÓĆ¹żŃõ»ÆĒāČÜŅŗŗĶ¶žŃõ»ÆĆĢÖĘČ”²¢ŹÕ¼ÆŃõĘų£¬ČōÓĆDŹÕ¼Æ£¬Ōņ¼ģŃéŃõĘųŹĒ·ńŹÕ¼ÆĀśµÄ²Ł×÷ĪŖ______________£¬ÖĘČ”ŃõĘų·“Ó¦µÄĪÄ×Ö±ķ“ļŹ½ĪŖ______________”£
£Ø4£©±Č½ĻÉĻŹöĮ½ÖÖÖĘČ”ŃõĘųµÄ·½·Ø£¬ĒėÖø³öÓĆ¹żŃõ»ÆĒāČÜŅŗŗĶ¶žŃõ»ÆĆĢÖĘČ”ŃõĘųµÄÓŵćÓŠ£ØŠ“Ņ»Ģõ¼“æÉ£©_____________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijøĘʬµÄ±źĒ©ČēĻĀ,ĒŅÖŖ“ĖøĘʬ³É·ÖÖŠÖ»ÓŠĢ¼ĖįøĘCaCO3ŗ¬ÓŠøĘŌŖĖŲ”£

£Ø1£©øßøĘʬ֊µÄ”°øĘ”±Ó¦Ąķ½āĪŖ ___________£ØĢīŠņŗÅ£©
¢ŁŌŖĖŲ ¢ŚŌ×Ó ¢Ū·Ö×Ó ¢Üµ„ÖŹ
£Ø2£©Ī¬ÉśĖŲÖÖĄą½Ļ¶ą,ĘäÖŠĪ¬ÉśĖŲD2µÄ»ÆѧŹ½ĪŖC28H44O,ŌņĪ¬ÉśĖŲD2µÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ_________£¬Ī¬ÉśĖŲD2ÖŠC”¢H”¢OČżÖÖŌŖĖŲµÄŌ×ÓøöŹżÖ®±ČĪŖ______
£Ø3£©Čē¹ūŅ»øöĒąÉŁÄźĆæĢģŠčŅŖ²¹øĘ0.8æĖ£¬ĘäÖŠ0.6æĖ¶¼Ą“×ŌÓŚÅ£ÄĢ£¬ĘäÓą·žÓĆøĘʬ”£Ēė¼ĘĖćĆæĢģĖūŠčŅŖ²¹³äĢ¼ĖįøʶąÉŁæĖ£æ£ØŅŖĒóÓŠ¼ĘĖć¹ż³Ģ£©________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»ÆѧÓļŃŌŹĒѧŗĆ»ÆѧµÄ»ł“””£ĒėŠ“³ö·ūŗĻŅŖĒóµÄ»Æѧ·ūŗÅ»ņŗ¬Ņ唣
¢Łŗ¤Ęų_______£»3øöŃõ·Ö×Ó_______£»![]() _______£»
_______£»![]() ________”£
________ӣ
¢Śµ¼ÖĀĖįÓźµÄĘųĢåŹĒ___________£»µ¼ÖĀĪĀŹŅŠ§Ó¦µÄĘųĢå__________”£
¢Ū»īŠŌĢæČ„³ż±łĻäÖŠµÄŅģĪ¶£¬ŹĒĄūÓĆĮĖĖüµÄ____________ŠŌ”£
¢Üµā¾ĘÖŠµÄČܼĮŹĒ__________£ØĢīĆū³Ę£©”£
¢ŻÉśŹÆ»ŅæÉŅŌ×÷”°ĶśĶśŃ©±ż”±øÉŌļ¼Į£¬ĘäŌĄķÓĆ»Æѧ·½³ĢŹ½±ķŹ¾_____________”£
¢ŽĒåĮ¹ÓĶÄÜ»īŃŖĻūÖ×”¢ÕņĶ“Ö¹Ń÷£¬ĘäÖ÷ŅŖ³É·ÖĪŖ±”ŗÉÄŌ£ØC10H1OO£©”£ĖüÓŠ______ÖÖŌŖĖŲ×é³É£¬ĘäĦ¶ūÖŹĮæŹĒ______£»Ģ¼”¢ĒāŌŖĖŲµÄÖŹĮæ±Č________£»ŃõŌŖĖŲĖłÕ¼µÄÖŹĮæ·ÖŹżŹĒ________£Ø¾«Č·µ½0.01%£©£»73g±”ŗÉÄŌµÄĪļÖŹµÄĮæŹĒ_______mol£¬1mol±”ŗÉÄŌ·Ö×ÓŌ¼ŗ¬_________øöĒāŌ×Ó”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com