

分析 本题属于推断题,根据题目给出的流程图和信息:黑色固体A碳在氧气中不充分燃烧生成一氧化碳,因此A是碳,B是一氧化碳;能与红色固体C高温反应生成D,D能与氧气反应,故D铁,C是氧化铜,生成的E是四氧化三铁;铁与铜的盐溶液反应生成红色的铜,因此F是铜.据此解答.
解答 解:黑色固体A碳在氧气中不充分燃烧生成一氧化碳,因此A是碳,B是一氧化碳;能与红色固体C高温反应生成D,D能与氧气反应,故D铁,C是氧化铜,生成的E是四氧化三铁;铁与铜的盐溶液反应生成红色的铜,因此F是铜.带入框图,推断合理;
(1)A是碳,故填:C;
(2)反应②是铁与铜盐溶液的反应,属于置换反应,故填:置换反应;
(3)反应①是一氧化碳与氧化铁高温反应生成铁和二氧化碳,故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
反应③可以是铁与硫酸铜反应生成硫酸亚铁和铜,故填:Fe+CuSO4=FeSO4+Cu.
点评 本考点属于物质的推断题,是通过对实验方法和过程的探究,在比较鉴别的基础上,得出了正确的实验结论.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
| 实验次数 | 1 | 2 | 3 | 4 |
| 加入样品的质量/g | 12.5 | 25 | 37.5 | 50 |
| 生成CO2 的质量/g | 4.4 | 8.8 | 11.6 | m |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
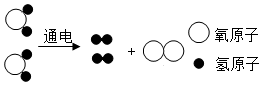 微粒观是化学的重要观念之一,宏观-微观-符号”之间建立联系,是化学学科特有的思维方式.如图是某化学反应的微观示意图
微粒观是化学的重要观念之一,宏观-微观-符号”之间建立联系,是化学学科特有的思维方式.如图是某化学反应的微观示意图查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
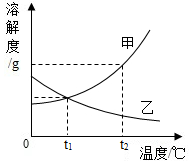 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com