
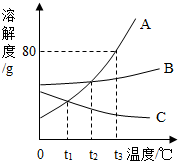
 如图是A、B、C三种物质的溶解度随温度变化的曲线图,据图回答下列问题.
如图是A、B、C三种物质的溶解度随温度变化的曲线图,据图回答下列问题.分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)据图可以看出,在t2℃时,A、B、C三种物质饱和溶液中溶质质量分数的大小关系是A=B>C,故填:A=B>C;
(2)t3℃时,A的溶解度是80g,将70gA物质加入到100g水中充分溶解,此时溶液中溶液、溶剂、溶质的质量比为170g:100g:70g=17:10:7,故填:17:10:7;
(3)将接近饱和的C溶液,使其达到饱和的方法是增加溶质、蒸发溶剂或是升高温度,故填:增加溶质、蒸发溶剂或是升高温度;
(4)B的溶解度随温度的升高变化不明显,故若从B的溶液中提取B,可采用的方法是蒸发结晶,故填:蒸发结晶;
(5)A的溶解度随温度的升高变化明显,故当A中混有少量B时,可以用降温结晶法提纯A,故填:降温结晶.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:初中化学 来源: 题型:多选题
| A. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | B. | 3Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | ||
| C. | 2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+O2↑ | D. | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com