
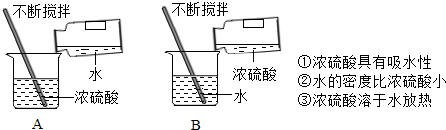
���� ��1��Ũ�����ϡ�ʹ���������˵����ָ��Ũ�����ˮ���ϡ����Ĺ��̣�������ˮ���ܶȽ�С������Ũ�������棬��Ũ��������ˮʱ��ų��������ȣ�ʹˮ���̷��ڣ��������Һ�������ܷɽ������Ƿdz�Σ�յģ���ˣ�Ũ����ϡ��ʱ��һ��ҪŨ��������������ע��ˮ��������ò��������裻�в��ɽ�ˮ����Ũ�����
��Ũ��Һ��ˮϡ��ǰ����Һ�����ʵ��������䣬����Ũ��Һ�����ʵ������ɼ����ˮϡ��ʱˮ��������
��2����ͭ�е�ͭ���ܺ�ϡ���ᷴӦ��������Ӧ��Ϊп��ϡ���ᣬ���Ծݴ˷�Ӧ�Ļ�ѧ����ʽ���м��㣮
��� �⣺��1������ˮ���ܶȽ�С������Ũ�������棬��Ũ��������ˮʱ��ų��������ȣ�ʹˮ���̷��ڣ��������Һ�������ܷɽ�������Ũ����ϡ��ʱ��һ��ҪŨ��������������ע��ˮ��������ò��������裮
��������ˮ������Ϊx
100g��98%=��100g+x����20%
x=390g
390g��390mL��
�ʴ��ǣ�B���ۣ�390��
��2����ͭ�е�ͭ���ܺ�ϡ���ᷴӦ���������ϡ�������������ģ����Կ���֪��ʣ��Ĺ���Ϊͭ��
����ԭ��ͭм��Cu������Ϊ3.5�ˣ�
����Һ����������п������Ϊx������Ϊy��п������Ϊz��
Zn+H2SO4�TZnSO4+H2��
65 98 161 2
z y x 0.2g
$\frac{161}{x}=\frac{2}{0.2g}$��$\frac{98}{y}=\frac{2}{0.2g}$��$\frac{65}{z}=\frac{2}{0.2g}$
x=16.1g��y=9.8g��z=6.5g��
������Һ��������9.8��20%=49g��
��Ӧ��������Һ��������49+6.5-0.2=53.5g
��Ӧ��������Һ�����ʵ���������$\frac{16.1g}{53.5g}$��100%=30.1%
�ʴ�Ϊ��3.5
���� �����㿼���˸��ݻ�ѧ����ʽ�ļ��㣬�������������ͻ�ѧ����ʽ���ۺ�Ӧ�ã����п��������о������ֵ����ͣ�����ʱҪע�⣺��ѧ����ʽҪд��ȷ��ʼ�ղ�Ҫ���������غ㶨�ɣ���������Ҫ�����ڼ������У�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧ����Һ��һ����Fe2+��SO42-��H2O | |
| B�� | ��Һһ����dz��ɫ | |
| C�� | ������һ����ͭ | |
| D�� | �����ķ�Ӧ�����û���Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
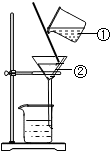 ��ͼΪijѧ�����д����ᴿʵ���й��˲���ʾ��ͼ���Իش�
��ͼΪijѧ�����д����ᴿʵ���й��˲���ʾ��ͼ���Իش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
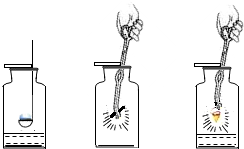 ������һ�ֻ�ѧ���ʱȽϻ��õ����壬�����Ժ��������ʷ�����ѧ��Ӧ����ͼ��ʾ��������̼��ϸ��˿��������ȼ�յ�������Ӧ������ȷ���ǣ�������
������һ�ֻ�ѧ���ʱȽϻ��õ����壬�����Ժ��������ʷ�����ѧ��Ӧ����ͼ��ʾ��������̼��ϸ��˿��������ȼ�յ�������Ӧ������ȷ���ǣ�������| A�� | ����Ҫ��������ˮ��ϸɳ | B�� | �����ﶼ�ǹ��� | ||
| C�� | ����������ɫ���� | D�� | ���Ϸ�Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com