
| 实验现象 | 化学方程式 | 结论 | |
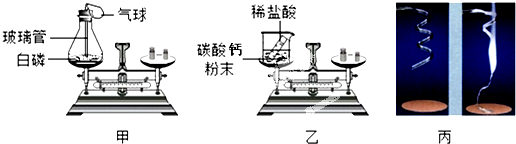
| 甲同学 | 白磷燃烧产生大量白烟,发光,放热,气球先膨胀后缩小;天平平衡 | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | 该实验遵守质量守恒定律 |
| 乙同学 | 烧杯中有大量气泡产生;天平不平衡. | CaCO3+2HCl=CaCl2+CO2↑+H2O | 该实验遵守质量守恒定律 |
| 丙同学 | 剧烈燃烧、发出耀眼白光、放热 生成 白色固体;反应前后称量质量不相等.(填“相等”或“不相等”) | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | 该实验不遵守质量守恒定律 |
分析 根据质量守恒定律内容分析解答:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和;
解答 解:(1)甲同学:在密闭的容器中,白磷和氧气反应生成了五氧化二磷,反应前后的质量相同,该实验能够验证参加化学反应的反应物的总质量和生成物的总质量相等.
乙同学:碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,由于有二氧化碳气体溢出,故反应后总质量比反应前总质量减少,观察到天平不平衡;所以现象为:烧杯内产生大量气泡,天平不平衡;
丙同学:镁条燃烧生成氧化镁,参加反应的是镁和氧气,生成的是氧化镁固体,生成的氧化镁固体质量等于参加反应的镁和氧气的质量和,但反应没有在密闭容器中进行了,所以燃烧后的总质量大于反应前的总质量,反应的方程式为:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
(2)磷燃烧的产物五氧化二磷和镁燃烧的产物氧化镁均是由两种元素组成,且其中一种是氧元素,故都是氧化物;
(3)天平不平衡的原因可能是有气体的参加反应或有气体、热量等的溢出,故答案为:反应前未称量参加反应的氧气的质量,反应后生成的氧化镁部分外溢,无法称量;
(4)从微观角度分析化学反应遵守质量守恒定律的原因是原子的“三个不变”,即化学反应前后原子的种类、数目、质量都没有发生改变.
故答案为:(1)见上表;(2)A; (3)反应前未称量参加反应的氧气的质量,反应后生成的氧化镁部分外溢,无法称量;(4)化学反应前后原子的种类、数目、质量都没有发生改变.
点评 要验证质量守恒定律需根据反应物的状态和产物的状态选择敞口或密闭装置,若有气体参加或生成的反应需在密闭容器中进行.


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:初中化学 来源:湖北省仙桃市2017届九年级中考模拟化学试卷 题型:选择题
根据右图提供的信息,下列说法正确的是
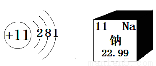
A.钠原子最外层有11个电子
B.钠的相对原子质量是22.99g
C.钠的原子序数为11
D.钠属于非金属元素
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 试剂 | 操作方法 |
| A | H2O | 悬浮物 | 过量的明矾 | 振荡、静止 |
| B | 铁粉 | 铁锈 | 过量稀盐酸 | 充分反应后过滤蒸发结晶 |
| C | CO2 | HCl | 足量硝酸银溶液 | 再通过盛有浓硫酸的洗气瓶 |
| D | NaCl溶液 | MgCl2 | 适量的氢氧化钠溶液 | 过滤、洗涤、烘干 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
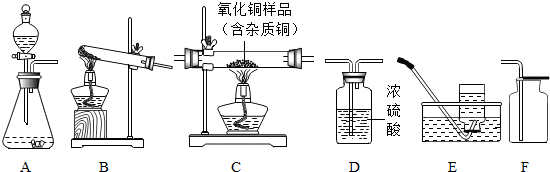
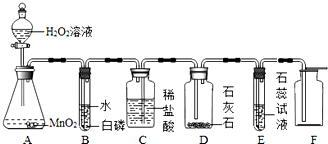 某同学利用“多米诺骨牌”效应,设计了如图气体制取与性质验证的组合实验,打开A中分液漏斗的活塞,很快看到E中导管口有气泡冒出,且溶液由紫色变红色.请看图回答问题:
某同学利用“多米诺骨牌”效应,设计了如图气体制取与性质验证的组合实验,打开A中分液漏斗的活塞,很快看到E中导管口有气泡冒出,且溶液由紫色变红色.请看图回答问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢气在氧气中燃烧时,产生淡蓝色的火焰 | |
| B. | 白磷在空气中燃烧时,产生大量白烟 | |
| C. | 镁条在空气中燃烧时,发出耀眼的强光 | |
| D. | 石蜡在氧气中燃烧时,生成水和二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
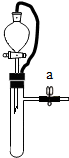 如图装置所示,实验室制取气体时常常在分液漏斗上方连接一个橡皮管,则橡皮管的作用最有可能的是( )
如图装置所示,实验室制取气体时常常在分液漏斗上方连接一个橡皮管,则橡皮管的作用最有可能的是( )| A. | 防止装置漏气 | B. | 防止液体流速过快,来不及收集 | ||
| C. | 便于检查装置气密性 | D. | 保持气压平衡,使液体顺利流下 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com