
【题目】在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水.某化学课外兴趣小组对碳的氧化物的成分进行了实验探究.
(提出问题)如何通过实验确定碳的氧化物的成分.
(猜想)
猜想1 | 猜想2 | 猜想3 |
只有CO | 只有CO2 | ______ |
(设计实验)基于猜想3,兴趣小组同学设计了如图实验装置:
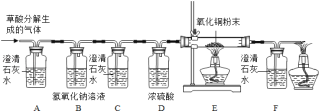
(实验探究)
(1)实验过程中观察到A装置中的澄清石灰水变浑浊,证明草酸分解时有CO2气体产生,A中发生的化学方程式为_______已知:氢氧化钠和氢氧化钙具有相似的化学性质。写出B中发生的化学方程式为______
(2)实验过程中还观察到以下实验现象:①C装置中澄清石灰水不变浑浊;②E装置中_____;③F装置中澄清石灰水变浑浊,证明有CO气体.
(实验结论)通过实验探究证明:猜想3成立.草酸分解的化学方程式是_______.
(问题讨论)
(1)C装置的作用是_______
(2)装置末端酒精灯的作用是尾气处理,写出发生反应的化学方程式_____。
(计算)某研究性学习小组的同学前往当地的石灰石矿区进行调查,他们取了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据见下表(杂质不溶于水,不与盐酸反应).
序号 | 第一次 | 第二次 | 第三次 | 第四次 |
加入稀盐酸质量g | 10 | 10 | 10 | 10 |
剩余固体质量g | 5.5 | 3.0 | 1.2 | m |
请计算:
(1)哪几次反应中碳酸钙有剩余________;
(2)上表中的m的数值应为________;
(3)这种石灰石中碳酸钙的质量分数为多少?(写出计算过程)______
【答案】CO和CO2 CO2+Ca(OH)2=CaCO3↓+H2O 2NaOH+CO2═Na2CO3+H2O 黑色粉末变成红色 H2C2O4![]() CO↑+CO2↑+H2O 检验二氧化碳是否被除尽 2CO+O2
CO↑+CO2↑+H2O 检验二氧化碳是否被除尽 2CO+O2![]() 2CO2 一、二 1.2 85%
2CO2 一、二 1.2 85%
【解析】
[猜想]碳的氧化物可能是一氧化碳,或二氧化碳,或一氧化碳和二氧化碳;故可根据猜想1、2的内容,推测猜想3的内容;故填:CO和CO2;
[实验探究](1)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水;氢氧化钠和二氧化碳反应生成碳酸钠和水,故填: CO2+Ca(OH)2=CaCO3↓+H2O;2NaOH+CO2═Na2CO3+H2O;
(2)C装置中澄清石灰水不变浑浊,说明原有的二氧化碳已经被完全吸收;E装置中黑色粉末变成红色,说明氧化铜被还原;F中澄清石灰水变浑浊,说明有二氧化碳生成,说明还原气是CO;故填:黑色粉末变成红色;
[实验结论]
草酸受热分解生成水、一氧化碳和二氧化碳,反应的化学方程式为:H2C2O4![]() CO↑+CO2↑+H2O。故填:H2C2O4
CO↑+CO2↑+H2O。故填:H2C2O4![]() CO↑+CO2↑+H2O;
CO↑+CO2↑+H2O;
[问题讨论]
(1)C装置的作用是检验二氧化碳是否被除尽。故填:检验二氧化碳是否被除尽;
(2)装置末端酒精灯的作用是尾气处理,发生的反应是一氧化碳在空气中燃烧生成二氧化碳,反应的化学方程式为:2CO+O2![]() 2CO2;故填:2CO+O2
2CO2;故填:2CO+O2![]() 2CO2;
2CO2;
[计算]
(1)每次加入的盐酸质量是相等的,但是第一、二次减少2.5g,第三次减少1.8g,所以第一次、第二次反应后碳酸钙质量有剩余;
(2)每次加入的盐酸质量是相等的,但是第一、二次减少2.5g,第三次只减少1.8g,说明碳酸钙完全反应,只剩余不和稀盐酸发生反应的杂质,所以第四次反应后剩余固体质量也是1.2g;
(3)通过第三次和的四次的数据可知:样品中杂质的质量为1.2g,所以石灰石中碳酸钙的质量分数为:![]() ×100%=85%.
×100%=85%.
故填:(1)一、二;(2)1.2;(3)85%.


科目:初中化学 来源: 题型:
【题目】人类文明的发展和社会的进步同金属材料关系十分密切。
(一)铁的应用及防护
(1)生活中常用铁锅烹饪,主要利用铁的_____(填字母)。
a 导电性 b 导热性 c 耐腐蚀
(2)“发蓝“处理是在铁表面形成致密氧化膜,以防止其腐蚀。“发蓝”的原理是:36Fe + 4NaNO2 + 9NaNO3 + 26H2O=12X + 13NaOH + 13NH3↑,X的化学式为_____
(3)患贫血症的人体内需要补铁 ____(填字母)。
a 分子 b 原子 c 元素
(4)如图为某兴趣小组探究铁生锈的三个实验,最先观察到铁锈的是____(选填序号)。

(5)铁生锈的主要过程为:
![]()
写出Fe(OH)2→Fe(OH)3反应的化学方程式______。
(二)铁的冶炼和探究
取20.0g Fe2O3粉末,小组同学用下图装置模拟炼铁,并测定反应后固体成分。
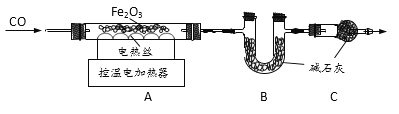
资料:碱石灰可吸收H2O和CO2。
(1)连接装置,先____,再装入药品。
(2)实验时先通入CO,目的是___。
(3)该实验装置有一个明显缺陷,你认为是___。
(4)控制A中温度在700℃至固体全部变黑,继续通CO至冷却。
①通过测定装置B中固体的质量变化,可准确求得装置A中剩余固体质量。装置C的作用是____。
②现直接测得装置A中剩余固体质量为17.2g。则装置B中固体应增重___g。
(5)经分析A中剩余固体17.2g为Fe和FexOy的混合物,向其中加入足量的稀H2SO4,充分反应,得H2 质量为0.1g。(FexOy和稀H2SO4反应,但无气体产生)
①固体中Fe质量为______g。 ②FexOy的化学式为____。
(三)成分探究
(查阅资料)用CO还原Fe2O3炼铁的过程大致分为三个阶段:
阶段1:3Fe2O3+CO![]() 2Fe3O4+CO2
2Fe3O4+CO2
阶段2:Fe3O4+CO![]() 3FeO+CO2
3FeO+CO2
阶段3:FeO+CO ![]() Fe+CO2
Fe+CO2
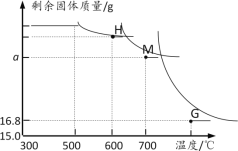
另取一定量Fe2O3进行上述实验,加热时固体质量随温度变化的曲线如图所示.回答下列问题:
(1)温度控制在300℃—500℃范围时,固体质量没有发生变化,原因是____。
(2)图中H点对应的固体成分的化学式是____
(3)图中M点对应a的数值=___
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组为探究生铁中铁的含量(生铁中只考虑铁,碳),设计有关方案,取0.58克生铁放于试管中,实验中将注射器内76毫升稀硫酸(足量)完全注入试管中。当试管中不再产生气泡时立刻读数得到量筒中水的体积为300毫升。已知实验条件下氢气的密度为0.09g/L。
(1)计算生铁中铁的质量分数?_____(写出计算过程,氢气质量保留两位小数,结果保留到0.1℅)
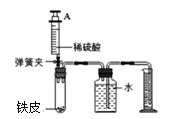
(2)上述方法测得的生铁中铁的质量分数偏小,可能的原因是_____。
A 没等装置冷却就读数 B 生铁中含有少量锌
C 试管中有氢气没有排出 D 将注射器中稀硫酸全部注入试管中后忘掉夹紧弹簧夹
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是有关氧气的知识网络图(反应条件部分省略),用化学用语填空:
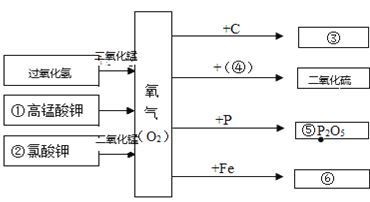
(1)物质①的化学式_____。
(2)物质②中的阳离子_____;②反应的化学方程式________________。
(3)物质③的化学式_____。
(4)物质④所含元素的符号_____。
(5)标出物质⑤化学式中带点元素的化合价_____。
(6)生成物质⑥的化学方程式__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前后各物质的质量分数如图所示。下列说法正确的是( )
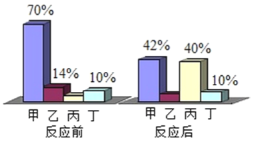
A. 丁一定是该反应的催化剂
B. 若消耗3g的乙,则生成17g的丙
C. 丙可能是单质
D. 甲、乙的质量之和一定等于生成丙的质量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】3月22日是“世界水日”,今年3月22-28日是第三十一届“中国水周”,珍惜水资源已经成为人们的共识。下列有关水的叙述正确的是()
A. 受热蒸发时水分子的体积逐渐变大,水由液态变为气态
B. 降温结冰时水分子静止不动,水的物理性质发生了变化
C. 参与光合作用的化学方程式为6CO2+6H2O![]() C6H12O6+602
C6H12O6+602
D. 电解生成氢气和氧气,说明反应时水分子中的原子种类发生了变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室利用如图所示装置进行相关实验,请回答问题。
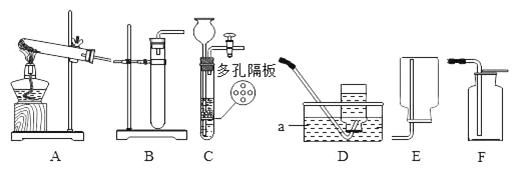
(1)写出装置图中标号 a 仪器的名称_______________________。
(2)用高锰酸钾制取氧气,选用的发生装置是_______________________。
(3)实验室里用锌粒和稀硫酸反应制取氢气,若要控制反应的发生和停止,应选用的________________发生装置是(填字母)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验课上,老师拿来一瓶久置的氢氧化钠溶液(以下简称A溶液)和一种初中常见的含 Ba2+的溶液(以下简称 B溶液),带领同学们一起进行实验探究。
(提出问题1)小四同学看到药品后,提出疑问:此氢氧化钠溶液可能已经变质,他的理由是_____(写化学方程式)。

(实验1)老师取少量A溶液于试管中加入适量B溶液,观察到______,说明此NaOH溶液已经变质。
(表达交流)小十同学看到老师的实验后,认为可向实验1的上层清液中加入酚酞溶液, 若无色酚酞溶液变红色,可确定A溶液中含有 NaOH,此瓶氢氧化钠溶液部分变质。小七同学不同意他的观点,理由是______
(提出问题2)将实验1所得的固液混合物过滤,所得滤液C中含有哪些离子?
(猜想假设)滤液C中一定含Na+,可能含 OH-、Cl-、NO3-
(实验探究)小雨同学取少量滤液C,进行如下实验:
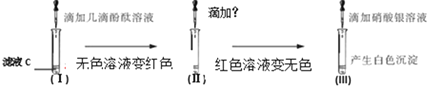
上述实验(Ⅱ)中需滴加______.
(实验结论)通过上述实验现象可确定溶液C中含有的离子是________,并由此确定了此氢氧化钠溶液变质程度和B溶液的成分。
(总结规律)通过探究我们可以认识到:检验溶液中两种及两种以上阴离子是否同时存在时,_____的离子要先验证,若存在要将其除去,再验证或结合已知信息 判断其他离子是否存在。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】宏观与微观是人类看待事物的两种基本视角。水在通电的条件下可以发生化学反应,请据图回答问题。
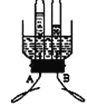
该图是同学们设计的电解水简易装置,其中A、B电极由金属曲别针制成。通电一段时间后,A和B两极的试管中产生气体的体积比为_____,电解水的化学方程式为_____,此实验说明水是由_____组成的。按要求写出一个与水有关的化学方程式,有水参加的化合反应:_____。请你从防止水污染、节约用水等方面写出一条自己力所能及的具体做法:_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com