
| A. | Cu和Mg | B. | Ag和Cu | C. | Zn和Cu | D. | Ag |
 备战中考寒假系列答案
备战中考寒假系列答案科目:初中化学 来源: 题型:解答题

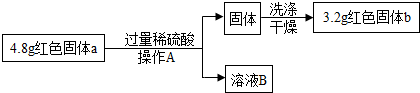
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 可用肥皂水区别硬水和软水 | |
| B. | 要保护水资源,只能禁止使用化肥和农药 | |
| C. | 为了控制空气中PM2.5的含量应停止建筑工地施工 | |
| D. | 因为有了温室效应,全球平均地表温度才提高到适合人类生存的15℃ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
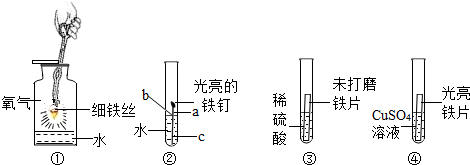
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 能源是人类生存和发展的基础,能源成为人们日益关注的问题.
能源是人类生存和发展的基础,能源成为人们日益关注的问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
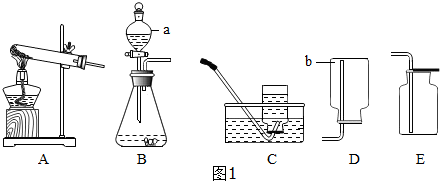
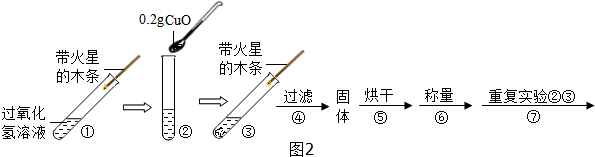
| 步骤③现象 | 步骤⑥结果 | 结论 |
| 带火星的木条复燃 | 固体质量是0.2g | 猜想Ⅰ、Ⅱ不成立 猜想Ⅲ成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com