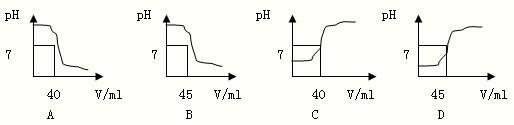
小明家购买了一瓶白醋,标签上注明醋酸的质量分数≥5%.小明想:这瓶白醋中醋酸的含量是否与标签的标注相符?请你用有关酸碱的知识,定量测定白醋中醋酸的含量.
一、【实验原理】:(1)用已知浓度的氢氧化钠溶液和醋酸反应,反应的化学方程式为:
CH3COOH+NaOH=CH3COONa+H2O
(2)在混合溶液中,当醋酸和氢氧化钠完全中和时,再增加1滴氢氧化钠溶液,溶液就呈碱性,而1滴氢氧化钠溶液约为0.05 mL,对测定结果的影响很小,可忽略不计.
二、【实验步骤】:(1)用________取12.0 mL白醋(密度近似为1.0g/mL),倒入烧杯中,加入20 mL蒸馏水稀释,再滴入几滴酚酞试液.
(2)量取45.0 mL溶质质量分数为1.0%的氢氧化钠溶液(密度近似为1.0 g/mL),用胶头滴管取该氢氧化钠溶液,逐滴地滴加到稀释后的白醋中,同时不断地搅拌烧杯中的溶液.滴至恰好完全反应,剩余氢氧化钠溶液5.0 mL.
三、【交流反思】:(1)在实验步骤:①中,加适量水稀释白醋,对实验结果有无影响?为什么?
(2)在实验步骤2 ②中,小明如何确定醋酸和氢氧化钠已完全中和?
四、【数据处理】:根据实验数据,通过计算判断白醋中醋酸的含量是否与标签的标注相符?(可能用到的相对原子质量:H-1,C-12,O-16,Na-23)
解:二、【实验步骤】:(1)量取液体的体积时需要用到量筒,故答案为:量筒
三、【交流反思】:(1)根据酸碱中和反应的实质,我们知道,加入水只是将溶液进行了稀释,而溶质的质量并没有发生变化,故答案为:没有影响,因为溶质的质量不变
(2)由于是测定白醋中醋酸的含量,所以要滴入滴入几滴酚酞试液作指示剂,酚酞试液遇酸不变色,遇碱变红色,根据指示剂颜色的变化来判断,反应的进行情况,故答案为:滴入最后一滴氢氧化钠溶液时,烧杯中液体由无色变红色
四、【数据处理】:根据有关化学方程式的计算步骤:一设、二写、三标、四列、五答,我们可以完成此题,由于计算结果x=5,标签上注明醋酸的质量分数≥5%,从而判断,这瓶白醋中醋酸的含量与标签的标注相符,故答案为:
解:设白醋中醋酸的质量分数为x%
CH3COOH+NaOH=CH3COONa+H2O
60 40
12mL×1.0g/mL×x% (45-5)mL×1.0g/mL×1.0%
60:(12mL×1.0g/mL×x%)=40:[(45-5)mL×1.0g/mL×1.0%]
解得:x=5
答:白醋中醋酸的质量分数与标签的标注相符.
分析:此题涉及到的是酸碱中和反应的计算问题,量取液体的体积时需要用到量筒,酸碱中和反应滴定终点的判断方法是根据滴定过程中指示剂颜色的变化来判断的,此题是滴入最后一滴氢氧化钠溶液时,烧杯中液体由无色变红色.
点评:此题所考内容能够抓住教材的重点,从多个角度考查学生的分析和解题能力,迎合了中考的考试方向,是中考的考点之一.