
| A. | 由①得原白色固体中一定不含FeCl3,一定含量有CaCO3 | |
| B. | 由②③得原白色固体中一定含有Ba(OH)2,一定不含量有Na2SO4 | |
| C. | 由实验现象判断,白色固体中至少有3种固体 | |
| D. | 由实验现象判断,白色固体的组成可有5种情况 |
分析 由于含Fe3+溶液呈黄色,其沉淀为红褐色,根据白色固体溶于水得到无色溶液A和白色沉淀B,可确定白色固体中不含FeCl3;
白色固体若只含两种物质,则根据(2)通入二氧化碳气体得到白色固沉淀,而在几种物质的溶液中,能与气体CO2反应形成沉淀的只有Ba(OH)2,也可以是NaOH、BaCl2或者NaOH、Ba(OH)2、BaCl2. 根据(3)中白色沉淀B全部溶于稀硝酸,可判断白色沉淀为CaCO3;确定不能存在硫酸钠.
解答 解:由于含Fe3+溶液呈黄色,其沉淀为红褐色,根据白色固体溶于水得到无色溶液A和白色沉淀B,可确定白色固体中不含FeCl3;
白色固体若只含两种物质,则根据(2)通入二氧化碳气体得到白色固沉淀,而在几种物质的溶液中,能与气体CO2反应形成沉淀的只有Ba(OH)2,也可以是NaOH、BaCl2或者NaOH、Ba(OH)2、BaCl2. 根据(3)中白色沉淀B全部溶于稀硝酸,可判断白色沉淀为CaCO3;确定不能存在硫酸钠.
白色固体若只含两种物质,则根据分析可以知道,固体A中一定含有CaCO3、Ba(OH)2,所以,若白色固体A中只含二种物质,它们是CaCO3、Ba(OH)2;
白色固体是由三种物质组成的,则白色固体A中一定含有CaCO3、Ba(OH)2或是氢氧化钠和氯化钡,一定不含FeCl3、Na2SO4,则白色固体含有三种物质,则可能的组成为:①CaCO3、Ba(OH)2、NaOH;②CaCO3、Ba(OH)2、BaCl2;③CaCO3、NaOH、BaCl2;
白色固体是由四种物质组成的,则白色固体A中一定含有CaCO3、Ba(OH)2、NaOH、BaCl2.
故选:D.
点评 根据物质的性质及变化规律,结合转化变化框图中的实验现象,确定固体中一定含有的物质与一定不含有的物质,然后对可能含有的物质进行组合.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
| 实验操作 | 实验现象及结论 |
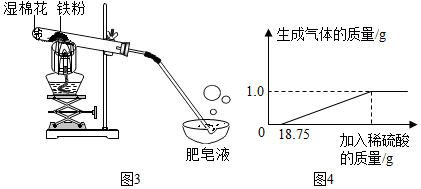
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 油锅着火用锅盖盖灭 | |
| B. | 睡觉时闻到很重的煤气味,打开电灯检查煤气罐漏气部位 | |
| C. | 室内起火时打开门窗通风 | |
| D. | 图书馆内图书起火,立即用泡沫灭火器扑灭 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
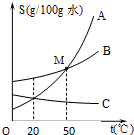 根据如图A、B、C三种固体的溶解度曲线回答:
根据如图A、B、C三种固体的溶解度曲线回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一定是乙烧杯中产生的氢气多 | |
| B. | 可能是乙烧杯中产生的氢气多 | |
| C. | 一定是甲烧杯中产生的氢气多 | |
| D. | 可能甲、乙两烧杯中产生的氢气一样多 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com