
由Mg(OH)2和MgO组成的混合物,测得其中含镁元素的质量分数为48%.取该混合物10 g,将其投入适量的稀硫酸中恰好完全反应,所得溶液中溶质的质量为
A.12 g
B.24 g
C.36 g
D.48 g
科目:初中化学 来源: 题型:阅读理解
| 煅烧 |
| 加水 |
| 物质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| 2mw |
| 21 |
| m(1-w) |
| 20 |
| 2mw |
| 21 |
| m(1-w) |
| 20 |
| 2mw |
| 21 |
| m(1-w) |
| 20 |
| 2mw |
| 21 |
| m(1-w) |
| 20 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 主族 周期 |
ⅢA | 0 | ||||||
| 1 | ||||||||
| 2 | A | B | ||||||
| C | D | E | ||||||
| F | G | H | ||||||
| J |
查看答案和解析>>
科目:初中化学 来源:2013年初中毕业升学考试(湖南衡阳卷)化学(解析版) 题型:计算题
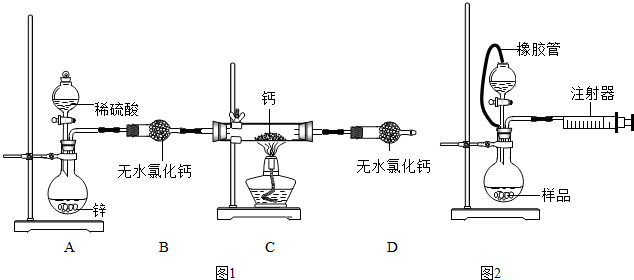
氢化钙(CaH2)固体是登山队员常用的能源提供剂.某化学兴趣小组拟用如图1所示的装置制备氢化钙,其反应的化学方程式为:Ca+H2 CaH2.
CaH2.

(1)CaH2中钙和氢元素的化合价分别为 ,装置中的无水氯化钙干燥装置也可用 来代替.
(2)利用该装置进行实验,步骤如下:检查装置的气密性后装入药品,打开分液漏斗活塞: (请按正确的顺序填入下列步骤的序号).
①加热反应一段时间 ②收集气体并检验其纯度 ③关闭分液漏斗活塞 ④停止加热,充分冷却
(3)为了确认进入装置C的氢气已经干燥,应在B、C之间再连接一装置X,装置X中加入的试剂是 .若氢气未充分干燥,装置X中的现象为 .
(4)为了测量上述实验中制得的氢化钙的纯度,该小组称取mg所制得样品,按如图2所示装置进行测定.旋开分液漏斗活塞,反应结束后充分冷却,注射器活塞由反应前的V1mL刻度处变化到V2mL刻度处(V2<V1,气体密度为dg/mL)
①橡胶管的作用为:a. ;b. .
②旋开分液漏斗活塞后,除发生CaH2+H2O═Ca(OH)2+H2↑的反应外,还最有可能发生的反应为 .
③用w表示氢化钙的纯度,请用一个等式表示出d、V1、V2和w之间的关系 .
④该小组乙同学认为去掉连接的注射器,也要计算出氢化钙的纯度.他同样称取mg样品,加入烧瓶中后称取反应前的质量为m1g,反应后的质量为m2g.乙同学表示出的m,m1,m2和w之间的关系的等式为 .
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
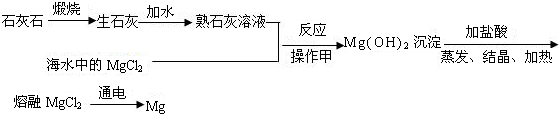
海洋是巨大的资源宝库,其中含有80多种元素。可以从海水中提取食盐,也可以从海水中提取用途广泛的金属镁,其制取工艺流程如下:

(1)从海水中提取食盐,是利用日光和风力使水分 ,得到食盐。
(2)要将Mg(OH)2沉淀分离出来,进行的操作甲的名称是 ,如果在学校实验室中完成该实验,要用到玻璃棒,其作用是 ,该操作中还需要的玻璃仪器是 和 。
(3)小明学习化学后知道,镁在氧气中燃烧会生成白色的氧化镁固体。但他在空气中点燃镁条时,却发现在生成的白色固体中还夹杂着少量的淡黄色固体。
[提出问题]为什么会生成淡黄色固体?
[查阅资料]小明查阅资料,记录了下列几种物质的颜色:
| 物 质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
其他同学认为不必查阅氯化镁的颜色,理由是 ;
[提出猜想]分析资料,小明认为淡黄色固体可能是由镁与空气中的 反应生成的;
[实验探究]小明设计实验证实了自己的猜想,他的方案可能是
;
[实验结论]根据小明的实验结果,写出镁条在空气中燃烧时两个反应的化学方程式: 、
[反思与评价]通过上述实验,你对燃烧有什么新的认识?
。
[知识拓展]由上述实验结果,若有12g镁在空气中完全燃烧,则所得产物的总质量m ___20g (填:“>”、“=”或“<”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com