
科目:初中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解


| 实验步骤 | 实验现象 | 实验结论 |
| a.取上述无色液体X少量于 试管中,至不再冒气泡为止, 加入足量的氯化钙溶液. |
产生白色沉淀 | 无色溶液X中含有 Na2CO3 Na2CO3 |
| b.取步骤a所得上层清液少量,滴加 稀盐酸 稀盐酸 |
没有气泡产生 没有气泡产生 |
无色溶液X中不含 NaHCO3 NaHCO3 |
查看答案和解析>>
科目:初中化学 来源:人教版初三年级上册原子的构成专项训练 题型:推断题
某实验小组对实验室中A、B、C、D四瓶无色溶液进行鉴别,它们分别是硫酸钠、稀硫酸、澄清石灰水、四种物质的一种。可供使用的实验用品有:稀盐酸、稀硫酸、碳酸钠、紫色石蕊溶液、硝酸钡溶液、硝酸银溶液、稀硝酸溶液、玻璃棒、试管、胶头滴管。请利用提供的实验用品,鉴别出四种物质,并完成实验报告:
| 实验 | 实验操作 | 实验现象 | 实验结论 |
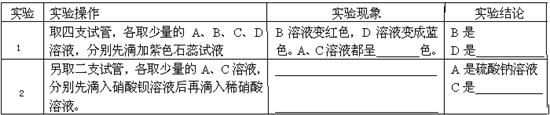
| ① | 取四支试管,各取少量的A、B、C、D溶液,分别先滴加紫色石蕊试液 | B溶液变红色,D溶液变成蓝色。A、C溶液都呈____色。 | B是________ D是________ |
| ② | 另取二支试管,各取少量的A、C溶液,分别先滴入硝酸钡溶液后再滴入稀硝酸溶液。 | ____________________ ____________________ _____________________ | A是硫酸钠溶液 C是________ |
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| ③ | 取该溶液少量试管E中,加入硝酸钡溶液后再加入稀硝酸酸 | 有白色沉淀生成 | 不能确定猜想______ 一定成立 |
| ④ | 取该溶液少量试管F中,加入加入稀盐酸,加热 | 有刺激性气味的气体生成 | 猜想____可能成立 |
| ⑤ | 在④所得的溶液中加入足量的________ | ______________________ | 猜想(3)成立 |
查看答案和解析>>
科目:初中化学 来源:人教新课标初三下册第十章酸和碱专项训练2 题型:实验探究题
某实验小组对实验室中A、B、C、D四瓶无色溶液进行鉴别,它们分别是硫酸钠、稀硫酸、澄清石灰水、四种物质的一种。可供使用的实验用品有:稀盐酸、稀硫酸、碳酸钠、紫色石蕊溶液、硝酸钡溶液、硝酸银溶液、稀硝酸溶液、玻璃棒、试管、胶头滴管。请利用提供的实验用品,鉴别出四种物质,并完成实验报告:
|
实验 |
实验操作 |
实验现象 |
实验结论 |
|
① |
取四支试管,各取少量的A、B、C、D溶液,分别先滴加紫色石蕊试液 |
B溶液变红色,D溶液变成蓝色。A、C溶液都呈____色。 |
B是________ D是________ |
|
② |
另取二支试管,各取少量的A、C溶液,分别先滴入硝酸钡溶液后再滴入稀硝酸溶液。 |
____________________ ____________________ _____________________ |
A是硫酸钠溶液 C是________ |
【发现问题】做完实验②后,该小组在网上查阅资料的时候发现,用稀硝酸酸化的硝酸钡溶液进行检验SO42-时,亚硫酸根离子(SO32-)的存在干扰了SO42-的检验。如往亚硫酸钠(Na2SO3 )溶液滴加硝酸钡溶液后有沉淀生成,再加足量的稀硝酸酸依然有白色沉淀。
【提出问题】若某无色溶液中可能含有硫酸根离子(SO42- )与亚硫酸根离子(SO32-)中的一种或两种,该如何检验?
【查阅资料】亚硫酸钡(Ba2SO3 )是无色晶体或白色粉末,微溶于水,在水中是白色沉淀。中性或碱性条件下NO3-不能和SO32-反应,但在酸性条件下,NO3-能和H+反应相遇时(HNO3 )具有强氧化性,易把SO32-氧化生成SO42- 。往亚硫酸钡中加入盐酸能发生类似于碳酸钡与盐酸的反应,生成有刺激性的气体。
【猜想】该无色溶液中含有(1)SO42- (2)SO32- (3)________。
【实验探究】请你将下列实验填写完整。
|
实验 |
实验操作 |
实验现象 |
实验结论 |
|
③ |
取该溶液少量试管E中,加入硝酸钡溶液后再加入稀硝酸酸 |
有白色沉淀生成 |
不能确定猜想______ 一定成立 |
|
④ |
取该溶液少量试管F中,加入加入稀盐酸,加热 |
有刺激性气味的气体生成 |
猜想____可能成立 |
|
⑤ |
在④所得的溶液中加入足量的________ |
______________________ |
猜想(3)成立 |
写出亚硫酸钠溶液与硝酸钡溶液发生复分解反应的化学方程式:________________。
【得出结论】要鉴别一种离子的存在,必须排除其它离子的干扰,不然会得出错误的结论。
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
(15分)某实验小组对实验室中A、B、C、D四瓶无色溶液进行鉴别,它们分别是硫酸钠、稀硫酸、澄清石灰水、四种物质的一种。可供使用的实验用品有:稀盐酸、稀硫酸、碳酸钠、紫色石蕊溶液、硝酸钡溶液、硝酸银溶液、稀硝酸溶液、玻璃棒、试管、胶头滴管。请利用提供的实验用品,鉴别出四种物质,并完成实验报告:
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| ① | 取四支试管,各取少量的A、B、C、D溶液,分别先滴加紫色石蕊试液 | B溶液变红色,D溶液变成蓝色。A、C溶液都呈 色。 | B是 D是 |
| ② | 另取二支试管,各取少量的A、C溶液,分别先滴入硝酸钡溶液后再滴入稀硝酸溶液。 |
| A是硫酸钠溶液 C是 |
【发现问题】做完实验②后,该小组在网上查阅资料的时候发现,用稀硝酸酸化的硝酸钡溶液进行检验SO42-时,亚硫酸根离子(SO32-)的存在干扰了SO42-的检验。如往亚硫酸钠(Na2SO3 )溶液滴加硝酸钡溶液后有沉淀生成,再加足量的稀硝酸酸依然有白色沉淀。
【提出问题】若某无色溶液中可能含有硫酸根离子(SO42- )与亚硫酸根离子(SO32-)中的一种或两种,该如何检验?
【查阅资料】亚硫酸钡(Ba2SO3 )是无色晶体或白色粉末,微溶于水,在水中是白色沉淀。中性或碱性条件下NO3-不能和SO32-反应,但在酸性条件下,NO3-能和H+反应相遇时(HNO3 )具有强氧化性,易把SO32-氧化生成SO42- 。往亚硫酸钡中加入盐酸能发生类似于碳酸钡与盐酸的反应,生成有刺激性的气体。
【猜 想】该无色溶液中含有(1)SO42- (2)SO32- (3) 。
【实验探究】请你将下列实验填写完整。
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| ③ | 取该溶液少量试管E中,加入硝酸钡溶液后再加入稀硝酸酸 | 有白色沉淀生成 | 不能确定猜想 一定成立 |
| ④ | 取该溶液少量试管F中,加入加入稀盐酸,加热 | 有刺激性气味的气体生成 | 猜想 可能成立 |
| ⑤ | 在④所得的溶液中加入足量的 |
| 猜想(3)成立 |
写出亚硫酸钠溶液与硝酸钡溶液发生复分解反应的化学方程式: 。
【得出结论】要鉴别一种离子的存在,必须排除其它离子的干扰,不然会得出错误的结论。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com