
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 | 39.0 | 39.8 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | 51.1 | 54.0 | 56.7 | |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.1 | 45.8 | 50.4 | 55.2 | 60.2 | 65.6 | 71.3 | 77.3 | |
| KNO3 | 13.3 | 20.4 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 202 | 246 | |
分析 (1)根据表格信息来分析;
(2)根据图表中四种物质的溶解度进行解答;
(3)复合肥料是指含有两种或两种以上营养元素的肥料;
(4)在考虑分离方法时通常要参考物质的溶解度受温度变化影响的大小.
(5)根据图表信息以及饱和溶液中溶质质量分数的计算方法来分析.
解答 解:(1)30℃时,MH4Cl的溶解度为41.1g;故填:41.1g;
(2)根据表格可以看出,氯化钠的溶解度随温度的升高变化不大,故填:NaCl;
(3)硝酸钾的组成中含有氮元素和钾元素,属于复合肥料,故填:KNO3;
(4)如果溶解度受温度影响较大的物质从溶液中结晶析出的方法是冷却热饱和溶液,如果溶解度受温度影响不大的物质从溶液中结晶析出的方法是蒸发溶剂.由于硝酸钾的溶解度受温度影响较大,氯化钠的溶解度受温度影响比较小,所以用降温结晶的方法提纯;故填:降温结晶;
(5)由表格信息可知,四种物质的溶解度均随着温度的降低而减小,故把1OO℃的NaCl、KCl、NH4Cl、KNO3饱和溶液降温至10℃时所得溶液均为饱和溶液,此时硝酸钾的溶解度最小,根据饱和溶液中溶质的质量分数=$\frac{溶解度}{溶解度+100g}×100%$可知,此时硝酸钾溶液中溶质的质量分数最小,故填:硝酸钾.
点评 本题难度不是很大,主要考查了固体溶解度表格所表示的意义,并能根据固体的溶解度表格解决相关的问题,从而培养学生分析问题、解决问题的能力.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:初中化学 来源: 题型:解答题
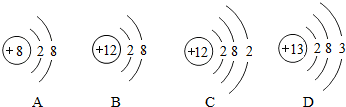
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
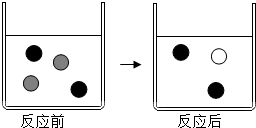 向AgNO3溶液中加入过量的铜粉充分反应,回答下列问题:
向AgNO3溶液中加入过量的铜粉充分反应,回答下列问题: Ag+、
Ag+、 Cu2+.
Cu2+.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 风助火威--为燃烧提供足够多的氧气 | |
| B. | 杯水车薪一水少了不能降低温度使温度低于可燃物的着火点 | |
| C. | 釜底袖薪一隔离可燃物可以灭火 | |
| D. | 水火不容--用水可以灭火,是因为降低了可燃物的着火点 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 小明同学利用一瓶敞口放置已久的NaOH溶液进行了一些实验探究.
小明同学利用一瓶敞口放置已久的NaOH溶液进行了一些实验探究.| 实验步骤 | 实验现象 | 结论 |
| (1)取样,滴加足量的CaCl2溶液. | 产生白色沉淀. | NaOH溶液部分变质. |
| (2)过滤,向滤液中滴加几滴无色酚酞试液. | 无色酚酞变红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 我们学习过常见气体的实验室制法,知道了制取气体的一般思路和方法.
我们学习过常见气体的实验室制法,知道了制取气体的一般思路和方法.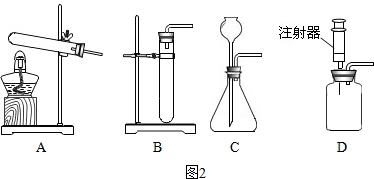
| 盐酸 | 大理石 | 温度条件 |
| 5% | 细颗粒 | 20℃ |
| 10% | 粗颗粒 | 40℃ |
| 每次用量均20mL | 每次用量均5g |
| 实验编号 | 温度 | 大理石规格 | HCl浓度 | 探究目的 |
| ① | 20℃ | 粗颗粒 | 5% | (I)实验①和②探究浓度对反应快慢的影响; (II)实验②和④探究温度对反应快慢的影响; (III)实验①和③③探究大理石粗、细对反应快慢的影响. |
| ② | 20℃ | 粗颗粒 | 10% | |
| ③ | 20℃ | 细颗粒 | 5% | |
| ④ | 40℃ | 粗颗粒 | 10% |
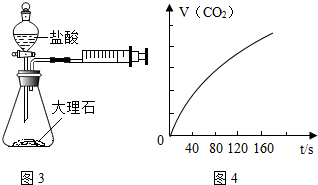 实验探究时,他们每次收集CO2气体均为40mL,则实验中他们还应记录的实验数据是收集40mL的CO2所需要的时间.图4是根据某次实验数据作出的CO2和时间变化的关系曲线,请分析在80秒以后,产生CO2逐渐减慢的可能原因:80秒后,盐酸反应了一部分,盐酸的浓度变低,反应速率变慢.
实验探究时,他们每次收集CO2气体均为40mL,则实验中他们还应记录的实验数据是收集40mL的CO2所需要的时间.图4是根据某次实验数据作出的CO2和时间变化的关系曲线,请分析在80秒以后,产生CO2逐渐减慢的可能原因:80秒后,盐酸反应了一部分,盐酸的浓度变低,反应速率变慢.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 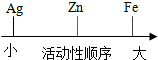 部分金属活动性顺序 | B. | 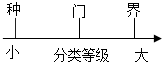 生物的分类等级 | ||
| C. | 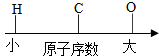 部分元素的原子序数 | D. | 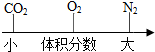 空气中部分成分的体积分数 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
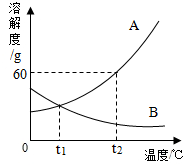 如图是A、B固体物质的溶解度曲线
如图是A、B固体物质的溶解度曲线查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com