
分析 (1)石灰石中碳酸钙高温下分解放出的二氧化碳使剩余固体质量减小,因此可利用质量守恒定律,求得分解放出二氧化碳的质量,利用质量与体积间关系,求得生成气体在标准善下的密度;
(2)石灰石样品的纯度即石灰石样品中碳酸钙的质量分数,根据分解反应的化学方程式,由放出二氧化碳的质量计算出样品中所含碳酸钙的质量及生成氧化钙的质量,求出石灰石样品的纯度.
解答 解:(1)根据质量守恒定律可知:
生成二氧化碳的质量为:22g-13.2g=8.8g.二氧化碳的体积为:$\frac{8.8g}{1.977g/L}$=4.45L
(2)设生成生石灰的质量为x.
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
56 44
x 8.8g
$\frac{56}{x}=\frac{44}{8.8g}$
x=11.2g
则所得产品的纯度为:(11.2g/13.2g)×100%=84.85%
答:(1)生成二氧化碳的质量是8.8g,这些二氧化碳的体积是4.45L;(2)制得生石灰的质量是11.2g,其产品的纯度是84.85%.
点评 解答时需要注意,剩余固体质量并非氧化钙的质量,其中还含有杂质,因此不能把此数据代入化学方程式进行碳酸钙质量的计算.


科目:初中化学 来源: 题型:选择题
| A. | 原子是构成物质的一种微粒 | |
| B. | 原子在化学变化中不能再分 | |
| C. | 原子是化学变化中最小的微粒,是因为原子质量小 | |
| D. | 分子是由原子构成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
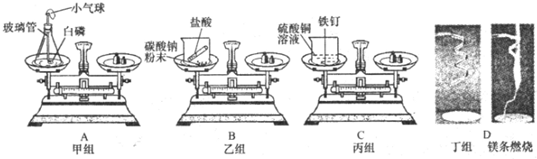
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
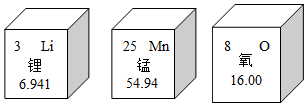
| A. | 锂是非金属元素 | B. | 锰的核内质子数为25 | ||
| C. | 氧的相对原子质量是16.00 | D. | 原子核外电子数Li>Mn>O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在潮湿、疏松、透气的土壤中 | B. | 在潮湿、疏松、透气的酸性土壤中 | ||
| C. | 在潮湿、致密、不透气的土壤中 | D. | 在干燥、致密、不透气的土壤中 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com