
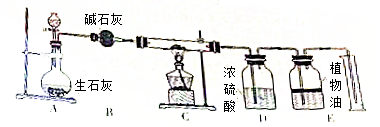
分析 (1)根据生石灰与水反应生成氢氧化钙,放出大量的热,进行分析解答.
(2)装置D中的药品是浓硫酸,具有吸水性,能与氨气反应;C中氨气与氧化铜反应生成铜、水,由质量守恒定律,同时还生成氮气,写出反应的化学方程式即可.
(3)氨气与氧化铜反应生成铜、水和水,由反应的化学方程式,氧化铜减少的质量即为氧化铜中氧元素的质量,进行分析解答.
(4)根据题意,氨气能与氧气反应,据此进行分析解答.
(5)装置D中浓硫酸吸收的是尾气中的氨气和生成的水蒸气,进行分析解答.
解答 解:(1)生石灰与水反应生成氢氧化钙,放出大量的热,装置A中生石灰的作用除了减少氨气中溶剂的外,还有的作用是利用生石灰与水放出大量的热,温度升高,
使氨气挥发出来.
(2)装置D中的药品是浓硫酸,具有吸水性,能与氨气反应,装置D的作用是吸收氨气和水蒸气.
C中氨气与氧化铜反应生成铜、水,由质量守恒定律,同时还生成氮气,反应的化学方程式为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$N2+3Cu+3H2O.
(3)氨气与氧化铜反应生成铜、水和水,由反应的化学方程式,氧化铜减少的质量即为氧化铜中氧元素的质量,称量mg样品放入质量为m1g的玻璃管中,冷却后关闭a并称量剩余固体及玻璃管的质量为m2g,则氧化铜中氧元素的质量为mg+m1g-m2g=(m+m1-m2)g,故氧化铜的质量为(m+m1-m2)g×$\frac{64+16}{16}$=5(m+m1-m2)g.
氧化铜样品中氧化铜的质量分数为$\frac{5(m+{m}_{1}-{m}_{2})g}{mg}$×100%=$\frac{5(m+{m}_{1}-{m}_{2})}{m}×100%$.
(4)氨气能与氧气反应,为防止加热时氨气与空气的混合气体在加热时发生爆炸,在点燃C处的酒精灯之前,要先通入氨气.
(5)装置D中浓硫酸吸收的是尾气中的氨气和生成的水蒸气,故不能通过测量装置D的增重量达到实验目的.
故答案为:(1)利用生石灰与水放出大量的热,温度升高,使氨气挥发出来;
(2)吸收氨气和水蒸气;2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$N2+3Cu+3H2O;
(3)$\frac{5(m+{m}_{1}-{m}_{2})}{m}×100%$;
(4)排出装置内的空气,发生加热时发生爆炸;
(5)装置D中吸收的是未反应的氨气和水蒸气,不能通过测量装置D的增重量达到实验目的.
点评 本题有一定难度,明确实验目的与反应原理、氧化钙的化学性质、化学方程式的书写方法、常见气体的性质等是正确解答本题的关键.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质的质量 | 甲 | 乙 | 丙 | 丁 |
| 反应前 | 25g | x | 5g | 5g |
| 反应后 | 8g | 23g | 5g | 8g |
| A. | 该反应是化合反应 | B. | x=9g | ||
| C. | 在该反应中,丙物质一定做催化剂 | D. | 在该反应中,甲丁的质量比为1:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用浓H2SO4干燥O2 | B. | 用熟石灰改良酸性土壤 | ||
| C. | 用灼烧的方法区别棉花和羊毛 | D. | 用纸盒代替铝制易拉罐盛装饮料 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
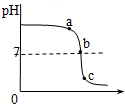 某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象如图所示.下列说法不正确的是( )
某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象如图所示.下列说法不正确的是( )| A. | 图中a点所示溶液能使紫色石蕊溶液变蓝 | |
| B. | 图中c点所示溶液中,含有的离子是Na+、H+、SO42-、OH- | |
| C. | 该实验是将硫酸逐滴滴入到盛有氢氧化钠溶液的烧杯中 | |
| D. | 此图象证明酸和碱发生了中和反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 表示氯原子,○表示氧原子,●表示氢原子;氧元素的化合价为-2价)
表示氯原子,○表示氧原子,●表示氢原子;氧元素的化合价为-2价)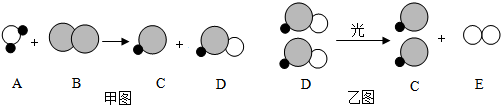
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com