


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
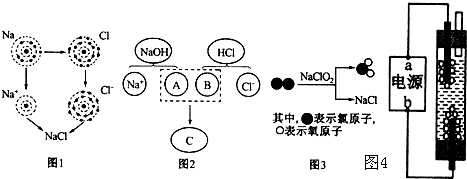
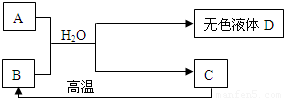
A为碳酸钠,C为相对分子质量为100白色不溶物,请填空:
(1)B常做食品干燥剂,理由(写化学方程式)_____________________________________
(2)D中一定含有的溶质是________________ ,检验D中是否含有A,可选用的试剂为______ (填下列序号)
a、酚酞溶液 b 、稀盐酸 c 、 澄清石灰水 d、pH试纸

(3)写出A、B和水三种物质的总反应的化学方程式___________________________________________________
(已知 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH)
查看答案和解析>>
科目:初中化学 来源: 题型:
氯化钠是重要的调味品,是舌尖上最不可缺少的味道.如图三幅示意图分别表示不同的化学反应,但生成物中都有氯化钠.
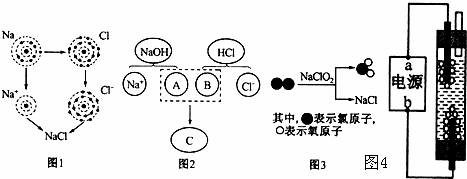
(1)图1是金属钠与氯气反应生成氯化钠的微观示意图.由图1可知,元素的化学性质主要与原子的 (填字母序号)有密切的关系;
A.最外层电子数
B.内层电子数
C.电子层数
D.相对原子质量
(2)图2描述了NaOH溶液与盐酸反应的微观实质,该反应的基本反应类型为 反应,图中A、B、C三种微粒的符号分别是 ﹣ 、 、 .向反应后的液体中滴加酚酞溶液,溶液呈无色.为探究反应后溶液中是否有盐酸剩余,所选试剂不正确的是 (填字母序号);
A.硝酸银溶液
B.锌粒
C.碳酸钠溶液
D.石蕊
(3)图3所示的四种物质中属于氧化物的是 (写化学式),该反应的化学方程式为 ;
(4)图4是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气,从能量变化角度看,该反应中将 能转化为化学能.该反应的化学方程式为2NaCl+2H2O 2NaOH+Cl2↑十H2↑,若电解含氯化钠23.4g的饱和食盐水,则可制得氢氧化钠的质量是多少?
2NaOH+Cl2↑十H2↑,若电解含氯化钠23.4g的饱和食盐水,则可制得氢氧化钠的质量是多少?
查看答案和解析>>
科目:初中化学 来源:2013年广东省珠海市文园中学中考化学一模试卷(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com