
 图甲表示元素周期表中的一种元素,该元素属于金属元素;(填“金属”或“非金属”);地壳中含量最多的金属元素与图乙表示的元素(元素符号为“O”)形成化合物的化学式是Al2O3.
图甲表示元素周期表中的一种元素,该元素属于金属元素;(填“金属”或“非金属”);地壳中含量最多的金属元素与图乙表示的元素(元素符号为“O”)形成化合物的化学式是Al2O3.  阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 | |
| 第一步 | 取部分该干燥剂于试管中,加水溶液 | 有放热现象 | 说明样品中含有氧化钙 |
| 第二步 | 向第一步的试管中滴加足量稀盐酸 | 有气泡出现 | 说明样品中含有碳酸钙 |
| 第三步 | 另取样品少许,加水溶解,然后滴加无色酚酞溶液 | 溶液变成红色 | 说明样品中含有氢氧化钙 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
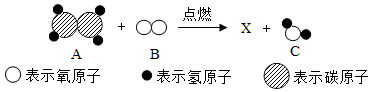
| A. | X的化学式为CO2,属于氧化物 | |
| B. | 参加反应的A与B的分子个数比为1:1 | |
| C. | 生成物质X与C的质量比为22:9 | |
| D. | 该反应的化学方程式可以表示C2H4+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+2H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 鉴别物质 | 实验方法 |
| A过氧化氢和蒸馏水 | 分别加入MnO2,看是否有气泡 |
| B镁和锌 | 分别加入稀盐酸,看是否有气泡 |
| C二氧化碳、氧气和空气 | 将燃着的木条分别伸入瓶中,观察现象 |
| D活性炭和氧化铜 | 分别投入盛有红棕色二氧化氮气体的集气瓶中,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水通电后生成氢气和氧气,说明水中含有氢元素和氧元素 | |
| B. | 冰块与水混合后得到纯净物 | |
| C. | 地球上可以利用的淡水资源有限 | |
| D. | 钠原子的质子数大于钠离子的质子数 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
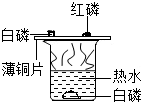 为研究可燃物燃烧的条件,设计了如下实验:在500毫升的烧杯中注入400毫升开水,并投入一小块白磷.在烧杯上盖一块薄铜片,铜片上一端放一小堆干燥的红磷,另一端放一小块已用滤纸吸去表面水的白磷(如图).
为研究可燃物燃烧的条件,设计了如下实验:在500毫升的烧杯中注入400毫升开水,并投入一小块白磷.在烧杯上盖一块薄铜片,铜片上一端放一小堆干燥的红磷,另一端放一小块已用滤纸吸去表面水的白磷(如图).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com