
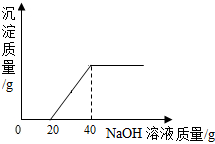
 向100g CuSO4与H2SO4的混合溶液中加入质量分数为20%的氢氧化钠溶液,产生沉淀的质量与所加氢氧化钠溶液的质量关系如图所示,回答下列问题:
向100g CuSO4与H2SO4的混合溶液中加入质量分数为20%的氢氧化钠溶液,产生沉淀的质量与所加氢氧化钠溶液的质量关系如图所示,回答下列问题:分析 (1)根据开始没有沉淀生成,说明硫酸过量,所以开始时硫酸和NaOH溶液反应生成硫酸钠和水进行解答;
(2)从图中可看出20g氢氧化钠溶液与混合溶液中的硫酸恰好完全反应,20g氢氧化钠溶液与混合溶液中的硫酸铜恰好完全反应.可利用氢氧化钠与硫酸铜反应的化学方程式,根据氢氧化钠的质量求出沉淀氢氧化铜的质量;
(3)所得溶液中溶质的质量分数=$\frac{溶质质量}{溶液质量}$×100%,溶质是硫酸钠,包括硫酸与氢氧化钠反应生成的硫酸钠和硫酸铜与氢氧化钠反应生成的硫酸钠;溶液的质量=所加入的所用物质的总质量-生成沉淀的质量.
解答 解:(1)根据开始没有沉淀生成,说明硫酸过量,所以开始时硫酸和NaOH溶液反应生成硫酸钠和水;
(2)设产生沉淀的质量为x,同时生成硫酸钠的质量为y,20g氢氧化钠溶液中溶质质量=20g×20%=4g
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
80 98 142
4g x y
$\frac{80}{4g}=\frac{98}{x}=\frac{142}{y}$
x=4.9g
y=7.1g
设与硫酸反应生成的硫酸钠质量为z,
2NaOH+H2SO4=Na2SO4+2H2O
80 142
20g×20% z
$\frac{80}{20g×20%}=\frac{142}{z}$
z=7.1g;
不饱和溶液中Na2SO4总质量为:7.1 g+7.1 g=14.2 g;
不饱和溶液的质量为:100 g+40 g-4.9 g=135.1 g;
所得不饱和溶液中Na2SO4质量分数:$\frac{14.2g}{135.1g}$×100%=10.5%
答案:
(1)H2SO4;
(2)生成沉淀Cu(OH)2的质量是4.9g;
(3)所得溶液中Na2SO4的质量分数是10.5%.
点评 本题主要考查学生利用化学方程式进行计算的能力.解题的关键是结合物质间反应的情况,正确分析图示数据,细心解答.


科目:初中化学 来源: 题型:选择题
| A. | 白玉为床金做马(《红楼梦》) | |
| B. | 春蚕到死丝方尽,蜡炬成灰泪始干(《无题》) | |
| C. | 爆竹声声一岁除,春风送暖人屠苏(《元日》) | |
| D. | 千锤万凿出深山,烈火焚烧若等闲(《石灰吟》) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


 和溶解度曲线回答下列问题:
和溶解度曲线回答下列问题:| 温度/℃ | 10 | 30 | 50 | 60 | |
| 溶解度/g | NaCl | 35.8 | 36.3 | 37.0 | 37.3 |
| KNO3 | 20.9 | 45.8 | 85.5 | 110 | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将地沟油转化为航空油,变废为宝 | |
| B. | 使用新型的可降解塑料,减少白色污染 | |
| C. | 改进汽车尾气净化技术,减少有害气体排放 | |
| D. | 加高化工厂的烟囱排放废气,防止形成酸雨 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
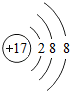 ,生成物NaClO中氯元素的化合价为+1.
,生成物NaClO中氯元素的化合价为+1.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 甲 | 乙 | 丙 | 丁 | 图例: --氢原子 --氢原子 --碳原子 --碳原子 --氧原子 --氧原子 |
| 化学式 | C | H2O | ? | H2 | |
| 微观 示意图 |  |  |  | ? |
| A. | 丙物质的化学式CO | B. | 丁物质微粒的微观示意图为○○ | ||
| C. | 保持甲化学性质的最小微粒是● | D. | 乙、丙、丁三种物质均由其分子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某中学综合实践活动小组在进行“诚信商品”研究时,检验商品标签所列成分及含量与实际是否相符.随机取出市售某种“纯碱”样品(成分说明见图),经检验杂质仅是氯化钠.准确称取样品10.9克,加入足量的氯化钙溶液使其完全反应,其反应式:Na2CO3+CaCl2=2NaCl+CaCO3↓.将反应生成的沉淀物经过滤,洗涤,烘干,干燥后得到CaCO3白色固体10克.请你完成以下计算:
某中学综合实践活动小组在进行“诚信商品”研究时,检验商品标签所列成分及含量与实际是否相符.随机取出市售某种“纯碱”样品(成分说明见图),经检验杂质仅是氯化钠.准确称取样品10.9克,加入足量的氯化钙溶液使其完全反应,其反应式:Na2CO3+CaCl2=2NaCl+CaCO3↓.将反应生成的沉淀物经过滤,洗涤,烘干,干燥后得到CaCO3白色固体10克.请你完成以下计算:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com