
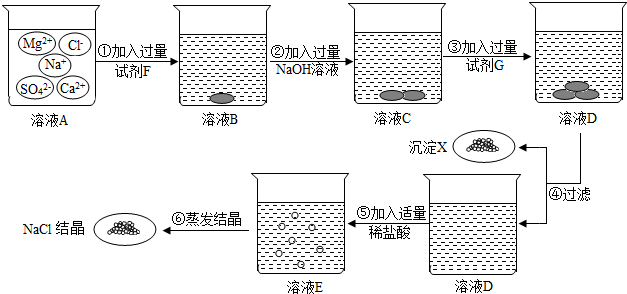
分析 根据除去溶液的MgCl2、CaCl2、Na2SO4,则用氢氧化镁除掉氯化镁,用氯化钡除掉硫酸钠,用碳酸钠除掉氯化钙与多余的氯化钡;在滤液中加盐酸的作用,应考虑除去NaOH、Na2CO3溶液进行分析.
解答 解:除去溶液的MgCl2、CaCl2、Na2SO4,则用氢氧化镁除掉氯化镁,用氯化钡除掉硫酸钠,用碳酸钠除掉氯化钙与多余的氯化钡;在滤液中加盐酸的作用,应考虑除去NaOH、Na2CO3溶液,所以
(1)欲除去粗盐中的可溶性杂质,步骤①中加入的试剂F是BaCl2,除去溶液中的硫酸钠;
(2)通过分析可知,加入的氯化钡是过量的,溶液B中,含有溶质是:MgCl2、CaCl2、NaCl、BaCl2;
(3)沉淀X中,含有硫酸钡、碳酸钡、碳酸钙、氢氧化镁4种沉淀;
(4)前面除杂加入的碳酸钠、氢氧化钠是过量的,所以溶液D中,存在的阴离子有C${{O}_{3}}^{2-}$、Cl-、OH-;
(5)步骤⑤中,发生的中和反应是氢氧化钠和盐酸反应生成氯化钠和水,化学方程式为:HCl+NaOH=NaCl+H2O;
(6)步骤④和步骤⑤不能对调,原因是:盐酸会与氢氧化镁、碳酸钙、碳酸钡沉淀反应.
故答案为:(1)BaCl2;
(2)MgCl2、CaCl2、NaCl、BaCl2;
(3)4;
(4)C${{O}_{3}}^{2-}$、Cl-、OH-;
(5)HCl+NaOH=NaCl+H2O;
(6)不能,盐酸会与氢氧化镁、碳酸钙、碳酸钡沉淀反应.
点评 掌握氯化钠与粗盐的提纯的方法及其注意事项;掌握一定溶质质量分数的溶液的配制方法;了解除杂和净化的方法.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | α-亚麻酸是由C、H、O三种元素组成的 | |
| B. | α-亚麻酸属于有机物 | |
| C. | α-亚麻酸分子中含氢元素的质量分数最高 | |
| D. | α-亚麻酸分子中C、H、O三种元素的原子个数比为9:15:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
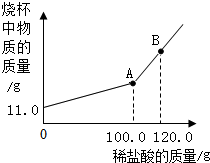 我国化工专家侯德榜发明了侯氏制碱法,为世界制碱工业作出了突出贡献.
我国化工专家侯德榜发明了侯氏制碱法,为世界制碱工业作出了突出贡献.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 中和反应有盐和水生成,但是有盐和水生成的反应不一定是中和反应 | |
| B. | 酸雨的pH小于7,所以pH小于7的雨水属于酸雨 | |
| C. | 碱溶液能使无色酚酞溶液变红,所以使酚酞溶液变红的溶液一定是碱溶液 | |
| D. | 氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe+2HCl═FeCl2+H2↑ | B. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | ||
| C. | CaO+H2O═Ca(OH)2 | D. | NaOH+HCl═NaCl+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com