
| A. | Mn+2HCl═MnCl2+H2↑ | B. | Mg+MnSO4═MgSO4+Mn | ||
| C. | Mn+Cu(NO3)2═Mn(NO3)2+Cu | D. | Fe+MnSO4═FeSO4+Mn |
分析 在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢;在金属活动性顺序中,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来;据此进行分析判断.
解答 解:A、金属锰在金属活动性顺序中位于铝和锌之间,铝、锌是氢之前的金属,则锰排在氢的前面,能和盐酸发生置换反应,故A不符合题意.
B、金属锰在金属活动性顺序中位于铝和锌之间,则镁排在锰的前面,能与MnSO4溶液发生置换反应,故B不符合题意.
C、金属锰在金属活动性顺序中位于铝和锌之间,锌的活动性比铜强,所以锰排在铜的前面,能和CuSO4溶液发生置换反应,故C不符合题意.
D、金属锰在金属活动性顺序中位于铝和锌之间,则锰的活动性比铁强,所以不能和MnSO4溶液发生置换反应,故D符合题意.
故选:D.
点评 本题难度不是很大,考查了金属活动性顺序的应用,掌握金属活动性顺序并能灵活运用是正确解答此类题的关键所在.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:计算题
| 加NaOH溶液的次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 剩余固体的质量/g | 17.3 | 14.6 | 11.9 | 9.9 | m |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 使用元素符号、化学式等化学用语,是为了增加化学科学的神秘色彩 | |
| B. | 人们根据不同的需求,通过控制反应条件,促进或抑制化学反应 | |
| C. | 为了更好地利用物质,可对物质进行分离或混合 | |
| D. | 物质本身没有好与坏之分,而人们对物质的利用却存在合理与不合理之分 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 稀有气体在通电时能发出不同颜色的光 | |
| B. | 氧气的化学性质比较活泼,易燃烧 | |
| C. | 二氧化碳有毒,含量增多会引起温室效应 | |
| D. | 氮气约占空气体积的21% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | $\frac{m+2n-e}{2}$ | B. | m+2n-e | C. | m+n-2e | D. | m+n-e |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
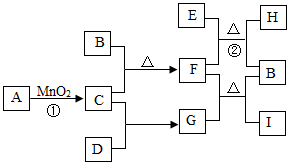
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲醛属于氧化物 | B. | 甲醛的相对分子质量是30g | ||
| C. | 甲醛中氢氧元素的质量比为2:1 | D. | 甲醛中氢元素的质量分数最小 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 阿司匹林是防止心血管病发生的常用药物,它具有抗血栓防止心肌梗塞等作用.阿司匹林又称乙酰水杨酸,化学式为C6H13O5N.
阿司匹林是防止心血管病发生的常用药物,它具有抗血栓防止心肌梗塞等作用.阿司匹林又称乙酰水杨酸,化学式为C6H13O5N.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com