
| 温度/℃ | 10 | 20 | 30 | 40 | |
| 溶解度 g/100gH2O | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
| 碳酸钠 | 12.2 | 21.8 | 39.7 | 53.2 | |
分析 ①由氯化钠和碳酸钠在不同温度时的溶解度表,查出40℃时氯化钠的溶解度即可;
②根据碳酸钠的溶解度受温度的影响变化大进行解答;
③由碳酸钠在不同温度时的溶解度表,确定碳酸钠的溶解度受温度影响的变化趋势即可.20℃时,碳酸钠的溶解度为21.8g,进行分析解答.
解答 解:①由图表可知40℃时,氯化钠的溶解度为36.6g.
②碳酸钠的溶解度受温度的影响变化大,所以碳酸钠溶液中混有少量的氯化钠,可通过降温结晶(或冷却热的饱和溶液)的方法提纯;
③由碳酸钠在不同温度时的溶解度表,碳酸钠的溶解度随温度的升高而增大.
20℃时,碳酸钠的溶解度为21.8g,在20℃时,将30g碳酸钠加入到100g水中,充分搅拌后,最多只能溶解21.8g,得到的是饱和溶液;
由表格知,30℃碳酸钠的溶解度为39.7g,将上述溶液升温到30℃,将100g的水加入30g碳酸钠中,充分搅拌后得到的是不饱和溶液,碳酸钠完全溶解,该溶液的溶质质量分数=$\frac{30g}{100g+30g}$×100%=23.1%.
故答案为:①36.6;②降温结晶(或冷却热的饱和溶液);③增大;饱和;23.1%.
点评 此题难度不大,掌握溶解度受温度影响的变化趋势、溶解度的含义是解题的关键.


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
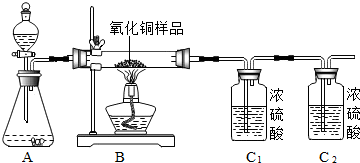
| 装置B中固体质量 | 装置C1的质量 | |
| 反应前 | 10.0克 | 150.8克 |
| 反应后 | 8.4克 | 152.8克 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 维生素在人体内起着重要的作用,是重要的供能物质 | |
| B. | 农业和园林灌溉,改大水浸灌为喷灌,滴灌有利于节约水 | |
| C. | 回收利用废旧金属、废旧书籍及废弃塑料完全没有必要 | |
| D. | 为了增加草莓产量,可以大量使用化肥农药 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
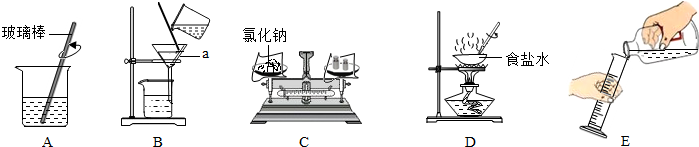
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
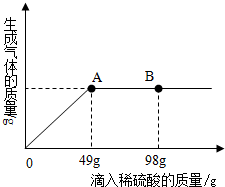 在一烧杯中盛有22.4gNa2CO3和Na2SO4组成的固体混合物,加入84克水使Na2CO3和Na2SO4全部溶解.向其中逐渐滴加溶质质量分数为20%的稀硫酸.生成气体的总质量与所滴入稀硫酸的质量关系曲线如下图所示,请根据题意回答问题:
在一烧杯中盛有22.4gNa2CO3和Na2SO4组成的固体混合物,加入84克水使Na2CO3和Na2SO4全部溶解.向其中逐渐滴加溶质质量分数为20%的稀硫酸.生成气体的总质量与所滴入稀硫酸的质量关系曲线如下图所示,请根据题意回答问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com