
【题目】如图为实验室制取气体的常见装置:
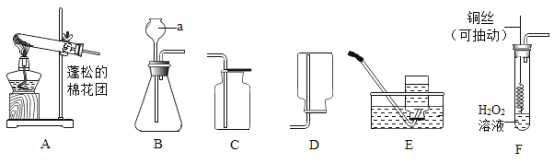
(1)制取和收集气体:任意写出一个实验室制氧气的化学方程式_____.利用该装置制氧气的发生装置为_____(选填“A ””B”)收集装置为_____(“C”“D”“E”),实验室制取二氧化碳的方程式为_____.
(2)实验改进:查阅资料发现,氧化铜可以做过氧化氢制氧气的催化剂,现有一根洁净的铜丝,实验前先绕成螺旋状,再经_____处理,改进后装置如图F所示,铜丝绕成螺旋状的目的是_____,将铜丝换成铜制的网兜,与改进前装置相比,改进后共同的优点是_____.
(3)温度、浓度、固体的颗粒大小等因素会影响反应速率.为研究实验室制取二氧化碳的适宜条件,进行如表四组实验:
实验编号药品 | 甲 | 乙 | 丙 | 丁 |
mg大理石 | 块状 | 块状 | 粉末状 | 粉末状 |
mg验算(过量) | 稀盐酸 | 浓盐酸 | 稀盐酸 | 浓盐酸 |
①实验甲与_____对照(填编号),是为了研究固体反应物颗粒大小对反应速率的影响;
②上述实验中,另一个影响反应速率的因素是_____.
【答案】2KMnO4![]() K2MnO4+MnO2+O2↑ A C或E CaCO3+2HCl=CaCl2+H2O+CO2↑ 灼烧或加热 增大与过氧化氢溶液的面积,加快反应速率 可以控制反应速率 丙 盐酸的浓度(反应物的浓度)
K2MnO4+MnO2+O2↑ A C或E CaCO3+2HCl=CaCl2+H2O+CO2↑ 灼烧或加热 增大与过氧化氢溶液的面积,加快反应速率 可以控制反应速率 丙 盐酸的浓度(反应物的浓度)
【解析】
(1)高锰酸钾制氧气反应原理:2KMnO4![]() K2MnO4+MnO2+O2↑;选择固体加热装置A,氧气密度比空气大,可以用向上排空气法收集氧气,选装置C;或者氧气不易溶于水,可以选择排水法收集氧气,选择装置E;实验室用大理石和稀盐酸制取二氧化碳气体的反应原理:CaCO3+2HCl=CaCl2+H2O+CO2↑;
K2MnO4+MnO2+O2↑;选择固体加热装置A,氧气密度比空气大,可以用向上排空气法收集氧气,选装置C;或者氧气不易溶于水,可以选择排水法收集氧气,选择装置E;实验室用大理石和稀盐酸制取二氧化碳气体的反应原理:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)氧化铜可以做过氧化氢制氧气的催化剂,现有一根洁净的铜丝,实验前先绕成螺旋状,再经灼热或加热处理,是铜变为氧化铜;改进后装置如图F所示,铜丝绕成螺旋状的目的:增大与过氧化氢溶液的面积,加快反应速率;将铜丝换成铜制的网兜,与改进前装置相比,改进后共同的优点:可以控制反应速率;
(3)由图表信息可知,利用控制变量法,①实验甲与丙对照,都使用稀盐酸,是为了研究固体反应物颗粒大小对反应速率的影响;
②上述实验中,另一个影响反应速率的因素是:稀盐酸的浓度(或反应物的浓度)。


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:初中化学 来源: 题型:
【题目】已知A、E、F是单质,B、C、D是化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成。其中B是相对分子质量最小的氧化物,D物质很不稳定,受热容易分解生成B和C,它们之间的转化关系如图所示。
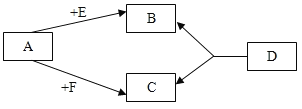
(1)则A的化学式为___,C的固体俗名为____。
(2)请你写出下列反应的符号表达式:D→B+C_____;反应基本类型为____。
查看答案和解析>>
科目:初中化学 来源: 题型:
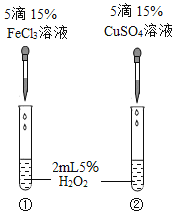
【题目】为比较Fe3+和Cu2+对过氧化氢分解反应的催化效果,某同学设计了如图所示的实验(FeCl3溶液、CuSO4溶液中都含有阴阳离子和水分子),有关实验有如下说法:
①过氧化氢中氧元素的化合价为-1价;
②若图1所示实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好;
③实验中可通过观察产生气泡快慢来比较反应速率;
④滴加FeCl3或CuSO4溶液后过氧化氢分解速率加快,则FeCl3或CuSO4是过氧化氢催化剂
以上说法不正确的是( )
A.①②B.①④C.②④D.③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列装置,结合所学化学知识回答下列问题。
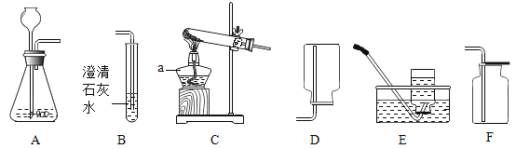
(1)写出仪器a的名称 。
(2)实验室用高锰酸钾制取氧气时,选择的发生装置是 (填字母序号),收集装置是 (填字母序号),发生反应的化学方程式为 。
(3)实验室用A装置制备二氧化碳的化学方程式为 。
(4)用B装置检验二氧化碳时,观察到澄清石灰水 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有以下仪器,请回答下列问题。

(1)图中标号仪器的名称:①_____②_____;
(2)如果称取一定质量的高锰酸钾放在大试管中,将温度控制在 250 ℃加热制取氧气。应选择的发生装置是_____(填字母);
其反应的化学方程式是_____;属于_____反应(基本反应类型);实验结束时,乙同学发现收集到的氧气大于理论产量,针对这一现象,同学们进行了如下探究:
(提出猜想)猜想Ⅰ:反应生成的二氧化锰分解放出氧气。
猜想Ⅱ:反应生成的锰酸钾分解放出氧气。
做出上述猜想的理由是_____。
(实验验证)同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的二氧化锰,控制在 250 ℃加热一段时间,冷却后测得二氧化锰的质量不变。则猜想_____错误。
②第二组同学取锰酸钾控制在 250 ℃加热一段时间,没有用测定质量的方法得出了猜想Ⅱ正确的结论。该组同学选择的实验方法是_____。
③实验结束后,发现水槽内的水变成了紫红色,可能的原因是_____(填字母)
A 氧气溶于水后形成的
B 水槽内的水就是紫红色的
C 管口没有棉花,高锰酸钾粉末通过导管进入水槽中
(3)如果用分解过氧化氢溶液来制取氧气
①应选择的发生装置是_____(填字母);
②其反应的化学方程式是_____;
③收集较纯净氧气的装置是_____;收集较干燥氧气的装置是_____(填字母);
④收集氧气的操作如下,其符合题意顺序为_____;
a.当气泡连续并比较均匀地放出时,再将导管口伸入盛满水的集气瓶
b.当气体收集满时,在水面下用玻璃片盖住瓶口移出水面正放在桌面上
c.将集气瓶盛满水,用玻璃片盖住瓶口,倒立在盛水的水槽内
(4)实验室用醋酸钠固体与碱石灰固体共热来制取甲烷。甲烷常温下是一种无色、无味的气体,密度比空气的小,极难溶于水。现选择合适的装置来制取并收集,应选择的发生装置是_____(填字母);收集装置是_____(填字母)。
(5)做铁丝在氧气中燃烧实验时要给铁丝系上一根火柴,其作用是_____;铁丝绕成螺旋状的目的是_____;瓶底铺上一层细沙,其作用是_____;铁丝在氧气中燃烧的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并填空。
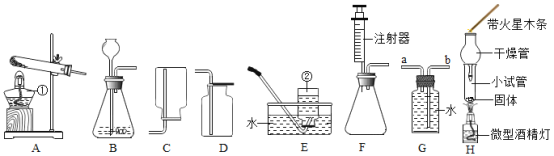
(1)写出带标号仪器的名称:① _________;②____________;
(2)若实验室用氯酸钾制取较纯净的氧气,应选用的装置组合是_______(填字母);若用G装置收集氧气,则氧气从______端(填a或b)进入。该反应的文字表达式是________________;
(3)某微型实验装置H如图,该装置相当于上图发生装置中的 _________(填字母),用该微型仪器进行实验,除试剂用量很少以外,还可能具有的优点是________________。(写出一点即可)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下是实验室常用的部分仪器。
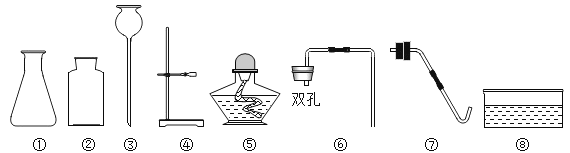
(1)写出下列仪器的名称②_____;⑤_____。
(2)某同学要用过氧化氢溶液和二氧化锰混合制取氧气,已经选择了仪器①②③,则还需要从图中选择的仪器是_____(填一种仪器的序号);反应的文字表达式为_____;该方法制取氧气的优点是_____。
(3)用上述方法制取氧气时,使用仪器③的需要注意_____。
(4)选择排水法收集气体时,判断集气瓶已收集满气体所依据的实验现象是_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小玲同学在探究二氧化锰在过氧化氢分解中作催化剂中,设计了以下探究实验。请根据题意答题
(1)实验报告
实验步骤 | 用带火星的木条检验时的现象 |
I.向试管①中倒入5mL30%的过氧化氢溶液 | 不复燃 |
Ⅱ.给试管①稍微加热,如图甲 | 不复燃 |
Ⅲ.向试管②中加入5mL30%的过氧化氢溶液和少量二氧化锰 | 产生大量气泡,带火星的木条复燃 |
(2)小玲在步骤Ⅱ的装置中,加装了一个U形管(如图乙装置)后,带火星的木条较易复燃。利用图甲装置做实验时,带火星的木条难复燃的原因是______________ ;改用乙装置后带火星的木条能够复燃,装置中冰水的作用是__________
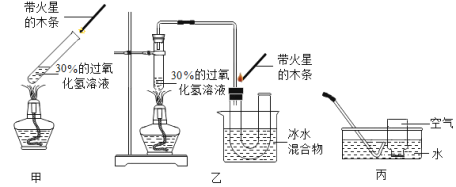
(3)小玲由此还想到了一个问题:能使带火星的木条复燃的气体一定是纯氧气吗?
小玲设计的实验如下:如丙图所示,按下表所示比例,用排水法收集部分氧气,分别得到五瓶空气和氧气的混合气体,进行木条复燃的实验。请你帮他将下表实验现象填写完全。
实验编号 | 空气体积分数% | 排水积分数% | 带火星的木条复燃情况 |
1 | 85 | 15 | 火星稍变亮,不复燃 |
2 | 80 | 20 | 火星明亮,时燃时不燃 |
3 | 75 | 25 | 复燃 |
4 | 70 | 30 | 复燃 |
5 | 50 | 50 | 复燃 |
通过以上实验,可以得出结论是__________小玲还能够粗略得出:使带火星的木条复燃的气体中氧气体积分数的范围是____________。
(4)小玲通过步骤Ⅲ得出二氧化锰能加快过氧化氢分解的结论,但小玮同学提出质疑:过氧化氢溶液由水和过氧化氢组成,也可能是二氧化锰加快水的分解产生氧气。请你设计一个实验证明小玮的猜想_____(请写出操作步骤和实验现象)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019年是元素周期表诞生150年,为了庆祝元素周期表诞生150周年,联合国宜布将2019年定为国际化学元素周期表年。下表是元素周期表部分元素的排列顺序,请依据图表回答下列问题:
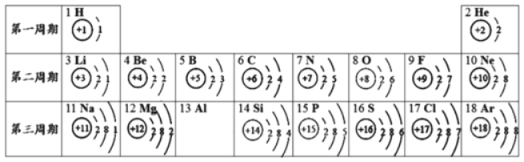
(1)磷和氧两种元素的最本质区别在于____________。
(2)如图是溴元素的原子结构示意图,根据其结构特点,可知溴元素与上表中的____元素化学性质相似。
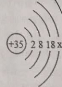
(3)原子序数为7的元素在化学反应中易________(填“得到”或“失去”)电子;该元素与原子序数为12的元素形成化合物的化学式为____________。
(4)在化学反应中,铝原子易失去电子形成铝离子,试画出铝离子结构示意图________。
(5)电池是高端电动汽车的主要动力源,其正极材料为LiCoO2,其中Co元素的化合价为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com