
化学小组同学对酸的性质很感兴趣,向老师提出研究硝酸的性质,老师高兴答应并带领同学们进行了硝酸性质的实验探究.
【实验设计】
(1)将石蕊试液滴入稀硝酸中,预计石蕊试液由紫色变 色.
(2)将Zn片投入稀硝酸中,预计将产生氢气.
【实验验证】同学们按上述设计做了实验,却发现石蕊变色后一会儿即褪去,Zn片投入稀HNO3后,溶液中冒出气泡,产生无色气体A,在试管口气体A变成红棕色有刺激性气味的气体B.
【提出问题】
(1)石蕊试液变色后为何会褪色?
(2)上述产生的无色气体是什么?硝酸具有哪些特性?
【查阅资料】看到如此异常的现象,在老师的指导下,同学们上网查到了下列资料:
(1)硝酸可与Zn、Cu等多种金属反应生成相应的硝酸盐,但不生成H2.
(2)含有氮元素的某些气态物质的物理性质
NH3 N2 NO NO2
顏色 无色 无色 无色 红棕色
溶解性 极易溶于水 不溶于水 不溶于水 可溶于水或硝酸
【猜想与分析】
(1)小明同学认为石蕊变色后又褪色的原因是由于试管不干净,含有其他杂质造成的,要证明小明的观点,应进行的操作是 .
(2)大家一致认同了红棕色气体B是NO2,但对于无色气体A及变化的原因有不同的看法:
①小丽同学认为A是NH3,但遭到大家的一致反对,原因是 ;
②小强同学认为A是N2,也遭到大家的一致反对,原因是 2 ;
③经讨论,最终大家获得了“A是NO”的共识.NO遇氧变成NO2的化学方程式为 .
【实验探究】小红同学对硝酸能与Cu反应很感兴趣,便取了一小块铜片投入稀HNO3中,发现Cu溶解,也出现上述Zn与稀HNO3反应的类似现象,确证生成了NO,并在老师的帮助下,测出恰好反应的Cu和HNO3的质量比为8:21,由此获得了Cu与稀HNO3的反应方程式为 .
【交流反思】根据探究结果可知,稀HNO3能跟铜反应的原因是硝酸具有氧化性.
【考点】实验探究物质的性质或变化规律;书写化学方程式、文字表达式、电离方程式.
【专题】简单实验方案的设计与评价;科学探究.
【分析】【实验设计】(1)依据石蕊遇酸性溶液的变色情况进行分析;
【猜想与分析】(1)设计一个干净的试管进行对比试验即可;
(2)①依据氨气极易溶于水,且不易被氧化分析判断;
②依据氮气化学性质很稳定分析判断;
③依据题干中的信息对化学方程式进行书写即可;
【实验探究】利用信息确定反应物与生成物,依据Cu和HNO3的质量比确定化学方程式中两者的化学计量数,并书写相关的方程式.
【解答】解:【实验设计】(1)石蕊遇酸性溶液会变红,稀硝酸溶液呈酸性所以石蕊会变红;
【猜想与分析】(1)设计一个干净的试管进行对比试验,从而确定是否是杂质影响了溶液颜色的变化,其操作为:取少量稀HNO3于干净的试管中,滴入石蕊试液.观察实验现象(或用干净的试管重复上述实验);
(2)依据氮元素某些气态物质的物理性质可知:
①氨气极易溶于水,且不易被氧化,所以该气体不可能是氨气;
②由于氮气化学性质很稳定,所以常温下N2在空气中不能氧化成NO;
③依据题干中的信息可知该反应的反应物是一氧化氮和氧气产物是二氧化氮,其方程式为:2NO+O2=2NO2.
【实验探究】由题干信息可知反应物是铜与硝酸与生成物是硝酸铜一氧化氮和水,此反应的方程是3Cu+8HNO3=3Cu (NO3)2+2NO↑+4H2O;
故答案为:【实验设计】(1)红.
【猜想与分析】(1)取少量稀HNO3于干净的试管中,滴入石蕊试液.观察实验现象;
(2)①NH3极易溶于水,大多数气体会溶解在稀HNO3中.且在常温下NH3不易被氧化成NO2.
②N2的化学性质比较稳定,常温下,N2在空气中不能氧化成NO2.
③2NO+O2=2NO2.
【实验探究】3Cu+8HNO3=3Cu (NO3)2+2NO↑+4H2O.
【点评】此题是一道实验探究题,实验探究题的常见模式一般是由题干提供新信息,然后利用这些新信息以及所学的知识对问题进行处理,从而训练学生获取信息并处理问题的能力.


科目:初中化学 来源: 题型:
找出物质之间的相互联系和区别,从中发现规律是我们学好化学的基本方法.
(1)如果将一氧化碳、氢气、酒精三种物质归为一类,则下列物质可纳入其中的是
A、氧气 B、二氧化碳 C、木炭 D、三氧化硫
(2)CO2、H2、O2、SO2四种物质按 的顺序可排列为H2<O2<CO2<SO2
(3)SO2、P2O5、CO、Al2O3、Fe3O4五种分子按 的顺序可排列为P2O5>Fe3O4>Al2O3>SO2>CO.
查看答案和解析>>
科目:初中化学 来源: 题型:
为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如下表:
第1次 第2次 第3次 第4次
加入稀硫酸质量(g) 100 100 100 100
剩余固体质量(g) 87 74 67.5 67.5
(1)第2次测得剩余固体质量为74g,其成分为 .
A.铜 B.锌 C.铜和锌
(2)该黄铜样品中铜和锌的质量比m铜:m锌: .
(3)计算所用稀硫酸的溶质质量分数,并画出反应生成的氢气质量与加入稀硫酸质量的关系图. 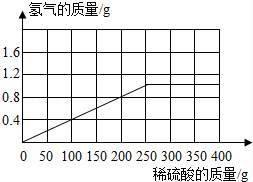
 .
.


查看答案和解析>>
科目:初中化学 来源: 题型:
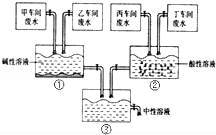
“五水共治”的首要任务是“治废水”,合理处理废水是当前防治废废水染的重要举措.某化工厂有甲、乙、丙、丁四个车间,排放的废水中分别含有FeCl3、HCl、Na2CO3、NaOH的一种.甲车间的废水呈黄色.通过调节废水流量,使乙、丁两个车间废水相对过量,通过如图方式处理,最终可使排出的废水呈中性.处理时第①反应池中出现大量的红褐色沉淀,第②反应池中出现大量的气泡.请回答:
(1)乙车间排放的废水主要成分是 .
(2)写出第②反应池的废水中的溶质有 .(用化学式表示)
(3)写出第③反应池中发生的化学反应方程式: .

查看答案和解析>>
科目:初中化学 来源: 题型:
在硫酸与硫酸铜的混合溶液200克中,滴入40%的氢氧化钠溶液100克,恰好完全反应.记录反应过程,得到的沉淀与所加的氢氧化钠溶液的质量关系如图所示.
(1)试分析在混合溶液中滴加氢氧化钠溶液时,为什么没有立即产生沉淀?
(2)当滴加50克氢氧化钠溶液时,混合溶液中的溶质是(用化学式表示) .
(3)200克混合溶液中,硫酸的溶质质量分数为 .
(4)完全反应时,所得溶液中的溶质质量分数为 .


查看答案和解析>>
科目:初中化学 来源: 题型:
化学物质及其变化与人类生产、生活密切相关,请填写下列空格:
(1)现有水、氮气、氧气、铁四中物质,其中:(填写化学式)
①可供给人类呼吸的是 .②可作溶剂,对生命活动具有重要作用的是 .
③可用于食品防腐的是 .④应用最广泛的金属是 .
(2)用化学方程式表示:
①水在通电作用下的反应:
②细铁丝在氧气中燃烧的反应: .
查看答案和解析>>
科目:初中化学 来源: 题型:
金属铬(Cr)是一种重要的金属材料,它具有良好的光泽度和抗腐蚀性,常用来镀在其它金属的表面上.小柯同学为了探究铬的性质,把金属铬放入硫酸铜溶液中,发现铬表面有红色物质生成.由此他可得出的结论是( )
A.铬比铜活泼
B.铬一定能与稀硫酸反应制得氢气
C.铬不能置换出硝酸亚铁中的铁
D.以上说法都正确
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com