
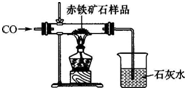
 (1)小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%.现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁98%的生铁的质量是2857t?(结果保留整数)
(1)小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%.现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁98%的生铁的质量是2857t?(结果保留整数)| 反应前 | 氧化铁完全反应后 | |
| A组 | 玻璃管和赤铁矿石样品的质量m1g | 玻璃管和固体物质的质量m2g |
| B组 | 烧杯和澄清石灰水的质量m3g | 烧杯和烧杯中物质的质量m4g |
分析 (1)根据CO还原氧化铁的反应化学方程式可得知,反应前氧化铁中铁元素全部被还原成生铁中的铁,因此,利用反应的化学方程式由氧化铁的质量可计算出生铁中铁的质量,然后再利用生成中铁的质量分数计算出所得生铁的质量;
(2)A组实验前后的质量差为被还原的氧化铁中氧元素的质量,由此数据可准确计算出铁矿石中氧化铁的质量及质量分数;而B组实验前后的质量差为石灰水吸收二氧化碳的质量,烧杯内的石灰水可能会吸收空气中二氧化碳而使质量差出现较大偏差而影响计算结果.
解答 解:(1)设得到生铁的质量为x
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
5000t×80% x×98%
$\frac{160}{5000t×80%}=\frac{112}{x×98%}$
x=2857t
答:理论上可炼出含铁98%的生铁的质量为2857t;
(2)A组实验中反应前后的质量差为被还原的氧化铁中氧元素的质量,由A组实验数据可准确计算出铁矿石中氧化铁的质量及质量分数;而B组实验中如果澄清石灰水吸收了空气中的二氧化碳,可使得反应前后质量差增大,影响根据二氧化碳质量所计算的氧化铁的质量及其质量分数,故不宜使用该组数据进行计算;
故答案为:(1)2857t (2)A;石灰水也会吸收空气中的二氧化碳,导致数据m4有误差.
点评 根据化学方程式进行计算时,所使用物质的质量应为纯净物的质量,含杂质的物质的质量不能直接代入方程式进行计算.


科目:初中化学 来源: 题型:解答题
 将 100g 稀盐酸慢慢加入到 24g 含有杂质的石灰石(杂质不溶于水也不与酸反应)中,反应情况如图所示.完成以下计算:
将 100g 稀盐酸慢慢加入到 24g 含有杂质的石灰石(杂质不溶于水也不与酸反应)中,反应情况如图所示.完成以下计算:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 一辆载有约30吨硝酸的罐车在某厂道路发生侧翻,硝酸泄露,散发出黄色烟雾,流到石灰石地面,发出嘶嘶声,产生大量气泡.泄露出来的硝酸不断流进路边的排水沟,气味十分刺鼻.
一辆载有约30吨硝酸的罐车在某厂道路发生侧翻,硝酸泄露,散发出黄色烟雾,流到石灰石地面,发出嘶嘶声,产生大量气泡.泄露出来的硝酸不断流进路边的排水沟,气味十分刺鼻.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
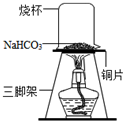 厨房中有一包无标识的白色粉末,经初步认定可能是氯化钠、碳酸钠、碳酸氢钠中的一种.小明对白色粉末的成分进行了探究.
厨房中有一包无标识的白色粉末,经初步认定可能是氯化钠、碳酸钠、碳酸氢钠中的一种.小明对白色粉末的成分进行了探究.| 实验步骤 | 实验内容 | 实验现象 | 实验结论 |
| 1 | 取少量溶液,滴加无色酚酞溶液 | 溶液变红色 | 白色粉末肯定不是NaCl |
| 2 | 取少量溶液,滴加稀盐酸 | 有气泡产生 | |
| 3 | 取少量溶液,滴加澄清石灰水 | 产生白色沉淀 |
| 序号 | 实验操作 | 预期现象 | 结论 |
| a | 取少量加热后的固体产物放入试管A中,加入适量蒸馏水,充分振荡溶解,滴加足量氯化钙,振荡,静置 | 产生白色沉淀 | 产物含Na2CO3 |
| b | 取操作①后的上层清液于试管B中,滴加酚酞 | 溶液不变色 | 产物不含NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物 质 | A | B | C | D |
| 反应前质量/g | 19.7 | 8.7 | 21.6 | 0.4 |
| 反应后质量/g | 待测 | 17.4 | 0 | 3.6 |
| A. | 物质C一定是化合物,物质D可能是单质 | |
| B. | 反应后密闭容器中A的质量为19.7g | |
| C. | 反应过程中,物质B和物质D变化的质量比为87:36 | |
| D. | 若物质A与物质C的相对分子质量之比为194:216,则反应中A和C的化学计量数之比为2:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 |
| ①取少量上层料液,滴加稀盐酸 | 无明显现象 |
| ②另取少量上层料液,滴加碳酸钠溶液 | 产生白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
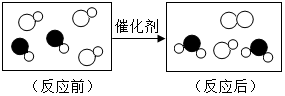 如图是“尾气催化转换器”将汽车尾气中有毒气体转化为无毒气体的微观示意图,其中不同的圆球代表不同的原子.下列说法错误的是( )
如图是“尾气催化转换器”将汽车尾气中有毒气体转化为无毒气体的微观示意图,其中不同的圆球代表不同的原子.下列说法错误的是( )| A. | 该反应没有单质生成 | |
| B. | 图中的反应物全部是化合物 | |
| C. | 参加了反应的两种分子个数比为1:1 | |
| D. | 生成物是一种单质和一种化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com