
���� ���ͨ���У��ٶ���ʹ��ɫʯ����Һ��죬����ʹ��ɫ��̪��ɫ�����ܹ��ͻ��ý�����Ӧ�������������ܹ��ͽ��������ﷴӦ�����κ�ˮ�����ܹ��ͼӦ�����κ�ˮ�����ܹ���ijЩ�η�Ӧ������������Σ�����Һ����������Һ�����ǵ�PH��С��7��
��� �⣺��1������Һ����������Һ���ʴ�Ϊ������
��2����������Һ���ܺ�ijЩ��������������ֽⷴӦ�����κ�ˮ���ʴ�Ϊ��Fe2O3+6HCl=2FeCl3+3H2O��
��3����ͼ�֮��ķ�Ӧ���кͷ�Ӧ���Ǹ��ֽⷴӦ��һ�֣��ʴ�Ϊ���кͣ��ֽ⣩��
��4������Ũ�������ǿ�ҵĻӷ��ԣ��ʴ�Ϊ��Ũ���
��5��������ת������ᣬ���������е����������ת��������ӣ�Ҳ���ǰ����������ת���ɳ��������Ӧ�����������Ȼ�����Һ���ʴ�Ϊ��H2SO4+BaCl2=2HCl+BaSO4����
���� �����ѶȲ��Ǻܴ���Ҫ����������йصĻ�ѧ���ʣ��Ӷ�����ѧ����֪ʶ��������õ�������


 С��ſ�ʱ��ҵϵ�д�
С��ſ�ʱ��ҵϵ�д� һ������ϵ�д�
һ������ϵ�д� �Ƹ�С״Ԫ���ֳ������ϵ�д�
�Ƹ�С״Ԫ���ֳ������ϵ�д� �¸��̵�ѧϵ�д�
�¸��̵�ѧϵ�д� ����ͬѧһ����ʦȫ�źþ�ϵ�д�
����ͬѧһ����ʦȫ�źþ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
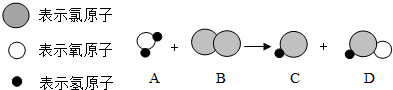
| A�� | �÷�Ӧ˵��ԭ���ڻ�ѧ��Ӧ�п��ٷ� | |
| B�� | ��Ӧ��ķ��Ӹ�����Ϊ3��2 | |
| C�� | ���в��뷴Ӧ�����ʶ��ǻ����� | |
| D�� | D��������Ԫ�صĻ��ϼ�+1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ʳ��ˮ���ݲ˵���ȥ��������� | B�� | ������ζ�ķ�������ƺͰ״� | ||
| C�� | ��ȼ�յķ���������ë�͵��� | D�� | �÷���ˮ������ˮ��Ӳˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������ˮ���������� | |
| B�� | ��ҵ��ˮֻҪ��ɫ���Ϳ���ֱ���ŷ� | |
| C�� | Ӳˮ����ˮû������ | |
| D�� | ũҵ���ᳫʹ��ũ�ҷʣ�����ʹ�û��ʺ�ũҩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | ���� | ���� | ţ�� | ������ |
| pH | 4.0��4.4 | 3.5��4.5 | 6.3��6.6 | 6.8��8.0 |
| A�� | ���� | B�� | ���� | C�� | ţ�� | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ú�����������ҩ������θ����� Al��OH��3+3HCl�TAlCl3+3H20 ���ֽⷴӦ | |
| B�� | �������о������ɷ� 2HgO$\frac{\underline{\;��\;}}{\;}$2Hg+O2 �ֽⷴӦ | |
| C�� | ����Ȼ����ȼ�� CH4+O2$\frac{\underline{\;��ȼ\;}}{\;}$CO2+2H2O ������Ӧ | |
| D�� | ��֤ͭ�����Ļ�� 3Cu+Al2��SO4��3�T3CuSO4+2Al �û���Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe��CO2��H3PO4 | B�� | H2��H2O��NaOH | C�� | O2��NaOH��H2SO4 | D�� | C��CaO��NaHSO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
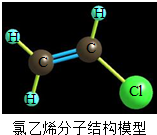 ������ϩ����д����PVC��������ϩ��һ�������¾ۺ϶��ɵģ�������ȼ���ͻ�ѧҩƷ�Ըߡ����Ե�����õ��ŵ㣮�������˵����ȷ���ǣ�������
������ϩ����д����PVC��������ϩ��һ�������¾ۺ϶��ɵģ�������ȼ���ͻ�ѧҩƷ�Ըߡ����Ե�����õ��ŵ㣮�������˵����ȷ���ǣ�������| A�� | һ������ϩ������̼���⡢������ԭ����� | |
| B�� | ����ϩ����������������������ȣ����Բ��Ե��� | |
| C�� | ������ϩ���л��߷��ӻ����� | |
| D�� | ������ϩ��̼����ԭ�ӵĸ�����Ϊ3��2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com