
【题目】(5分)碳酸钠和碳酸氢钠是生活中常见的两种白色固体。同学们对鉴别这两种物质非常感兴趣,
进行如下探究。
【查阅资料】
1.碳酸钠和碳酸氢钠在不同温度下的溶解度
10℃ | 20℃ | 30℃ | 40℃ | |
Na2CO3 | 12.5 g | 21.5 g | 39.7 g | 49.0 g |
NaHCO3 | 8.1 g | 9.6 g | 11.1 g | 12.7 g |
2.碳酸钠和碳酸氢钠化学性质(部分)的比较
性质 | Na2CO3 | NaHCO3 | 性质比较 |
溶液的酸碱性 | 碱性 | 碱性 | 相同条件下,Na2CO3溶液的碱性更强 |
热稳定性 | 稳定 | 不稳定 | NaHCO3受热分解生成Na2CO3、CO2和H2O |
与盐酸反应 | 反应 | 反应 | 均产生CO2,但NaHCO3与盐酸的反应更加剧烈 |
【设计方案并实施】
实验方案 | 实验现象及结论 |
方案一:___________ | 若有白色固体剩余,样品为碳酸氢钠;否则为碳酸钠。 |
方案二:分别将两种白色固体溶于水制成5%的溶液,___________,将其与标准比色板对照。 | pH值大的为碳酸钠溶液,pH值小的为碳酸氢钠溶液。 |
方案三:分别取少量固体于试管中加 热,然后将产生的气体通入石灰水中。 | ____________ |
方案四:如下图所示,分别将气球中的固体粉末全部且同时倒入装有过量盐酸的试管中,观察现象。
| ___________________________ |
【实验反思】
通过上述实验,我们知道根据物质的性质设计并进行______实验,能帮助我们更好地理解和掌握相关物质的性质。
【答案】
实验方案 | 实验现象及结论 |
方案一:20 ℃时,在100 g水中加入11 g该白色固体,充分溶解。 | |
方案二:用玻璃棒分别蘸取少量待测液于pH试纸上,静置,观察现象。 | |
若石灰水变浑浊,样品为碳酸氢钠,否则为碳酸钠。 | |
气球胀大速度快且大的,原固体为碳酸氢钠,否则为碳酸钠。 |
【实验反思】对比
【解析】
试题分析:根据资料中表1,碳酸钠和碳酸氢钠在不同温度下的溶解度,在相同的温度下,碳酸氢钠的溶解度比碳酸钠的要小,故可选择表中所提供的四个温度值来设计,方案一:20 ℃时,在100 g水中加入11 g该白色固体,充分溶解,现象及结论:若有白色固体剩余,样品为碳酸氢钠;否则为碳酸钠
根据表2中的信息,相同条件下,Na2CO3溶液的碱性更强,故方案二:用玻璃棒分别蘸取少量待测液于pH试纸上,静置,观察现象,pH值大的为碳酸钠溶液,pH值小的为碳酸氢钠溶液
根据表2中的信息,NaHCO3受热分解生成Na2CO3、CO2和H2O,故方案三:若石灰水变浑浊,样品为碳酸氢钠,否则为碳酸钠
根据表2中的信息,碳酸钠和碳酸氢钠虽然都能与盐酸反应,但NaHCO3与盐酸的反应更加剧烈,且根据化学方程式:Na2CO3+2HCl==2NaCl+H2O+CO2↑中Na2CO3与CO2的质量关系为106:44,而NaHCO3+HCl==NaCl+H2O+CO2↑中NaHCO3与CO2的质量关系为84:44,故相同质量的碳酸钠和碳酸氢钠,碳酸氢钠生成的二氧化碳质量更大,故方案四:如下图所示,分别将气球中的固体粉末全部且同时倒入装有过量盐酸的试管中,观察现象:气球胀大速度快且大的,原固体为碳酸氢钠,否则为碳酸钠
【实验反思】通过上述实验,我们知道根据物质的性质设计并进行对比实验,能帮助我们更好地理解和掌握相关物质的性质


科目:初中化学 来源: 题型:
【题目】(14分)实验室有几瓶未知浓度的氢氧化钠溶液,某兴趣小组同学欲用1%的稀盐酸来测定其溶质的质量分数。以下是几组同学的设想和做法:
(1)(7分)甲组同学的实验如下图所示:在烧杯中加入5g氢氧化钠溶液,滴入几滴酚酞溶液,用滴管慢慢滴入1%的稀盐酸,并不断搅拌,至溶液颜色恰好变为无色为止。
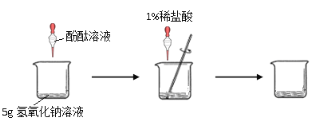
请回答:
①酚酞溶液的作用是 ;
②氢氧化钠与盐酸反应的化学方程式为 ;
③当溶液颜色恰好变为无色时,共用去了稀盐酸7.3g,试求甲组这瓶氢氧化钠溶液中溶质的质量分数和反应后所得溶液中溶质的质量分数 (写出计算过程,结果用百分数表示)。
(2)(5分)乙组同学的设想是:在烧杯中加入一定量的氢氧化钠溶液,用滴管慢慢滴入1%的稀盐酸,并不断搅拌,通过用pH试纸多次测定溶液pH的办法,达到实验目的。
①下列使用pH试纸的方法正确的是 (填字母)。
A.将pH试纸剪成几段节约使用
B.将pH试纸直接插入待测液中
C.将pH试纸放在干净的白瓷板上,用玻璃棒蘸取待测液滴在pH试纸上
D.将pH试纸用蒸馏水润湿后放在玻璃片上,用玻璃棒蘸取待测液滴在pH试纸上
②由于用pH试纸需多次测定,较繁琐,且所测数值不够精确。在老师指导下,乙组同学取了5g氢氧化钠溶液进行了数字化实验,由计算机描绘出了整个实验过程中溶液pH的变化图像(简单表示为下图)。
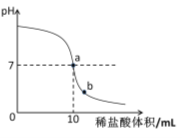
请回答:图中a点表示的含义是 ;b点溶液中的溶质有 (填化学式);乙组同学要计算出本组这瓶氢氧化钠溶液中溶质的质量分数,除了要用到已有数据外,你认为还需要的数据是 。
(3)(2分)丙组同学在滴加稀盐酸一段时间后,发现溶液中有少量气泡产生。这一“异常现象”激起了他们的探究欲望,通过实验证明:该组用的这瓶氢氧化钠溶液已经部分变质。请用化学方程式表示其变质的原因 ;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】茶叶中含有茶氨酸(C7H14O3N2,又称谷氨酰乙胺),它有降低血压、提高记忆力、保护神经细胞、减肥等效果。下列有关它的说法中,正确的是
A.茶氨酸中含有1个氮分子
B.茶氨酸的相对分子质量为174 g
C.茶氨酸中氧元素的质量分数为12%
D.茶氨酸由C、H、O、N四种元素组成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】谚语诗词中蕴含着科学道理.下列说法正确的是
A.“真金不怕火炼”是说黄金熔点很高
B.“众人拾柴火焰高”是指可燃物越多,着火点越低,越容易着火
C.“千锤万凿出深山,烈火焚烧若等闲”中发生的变化只有化学变化
D.“满架蔷薇一院香”的原因是分子在不停地运动
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(3分)生活离不开水,净化、软化水的知识在日常生活中有着广泛应用。
(1)茶杯内的纱网,可将茶叶与茶水分离,便于饮用,该设计利用的化学原理是 。
(2)井水中含有较多的钙、镁离子,硬度较大,为降低硬度,生活中可采用的方法是 。
(3)自来水厂可用二氧化氯(ClO2)消毒杀菌,ClO2中氯元素化合价为
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(7分)某科研所成功利用染化厂的废料铁泥(主要成分是Fe2O3、FeO和铁)制备可用于隐形飞机涂层的纳米四氧化三铁。
(1)在物质分类中,四氧化三铁属于 (填写物质类别)。在Fe2O3、FeO和Fe3O4三种物质中,铁元素的质量分数最高的是 。
(2)制备过程中要用到双氧水(过氧化氢溶液),其中双氧水的用量、调节的pH、反应时间是三个关键条件,研究时需要进行七组实验。若实验序号1是该制备过程的理论最佳制备条件,请在下表中填入实验序号为5、6、7的三组实验条件(与1-5组实验条件不同)。
实验序号 | 双氧水(mL) | pH | 反应时间(h) |
1 | 0.6 | 10 | 3 |
2 | 0.5 | 10 | 3 |
3 | 0.7 | 10 | 3 |
4 | 0.6 | 11 | 3 |
5 | |||
6 | |||
7 |
(3)调节溶液的pH可用碳酸钠或碳酸氢钠。
查阅资料可:2NaHCO3![]() Na2CO3 +CO2↑+ H2O,此反应的基本类型是 ,此反应证明NaHCO3的热稳定性 Na2CO3(填“大于”或“小于”)。
Na2CO3 +CO2↑+ H2O,此反应的基本类型是 ,此反应证明NaHCO3的热稳定性 Na2CO3(填“大于”或“小于”)。
[注意:若答对以下问题可奖励4分,化学试卷总分不超过60分。]
请你根据以上性质设计实验方案鉴别Na2CO3 和 NaHCO3固体。 。
试写出实验方案中另一个化学反应方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com