
分析 (1)根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
(2)根据金属活动顺序表知:锌>铜>银,所以加入锌粉,首先锌粉和硝酸银溶液反应,置换出单质银,如果锌粉足量可以再继续和硝酸铜反应置换出铜.若溶液呈无色,说明了溶液中无硝酸铜,据此分析判断;
(3)根据金属活动顺序表知:镁>铁>铜,所以加入镁粉,首先镁粉和氯化铜溶液反应,置换出单质铜,如果镁粉足量可以再继续和氯化亚铁反应置换出铁.据此分析判断.
解答 解:(1)铁的活动性比铜强,铁与硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;
(2)由题意可知金属活动性顺序可知,锌>铜>银.向含有AgNO3、Cu(NO3)2的混合液中加入一定量的锌粉,锌粉会首先置换硝酸银中的银,待硝酸银完全反应后继续与硝酸铜发生反应.若溶液呈无色,说明溶液中Cu(NO3)2、AgNO3,完全反应,即原混合溶液中的银和铜全部被置换出来,则滤出的固体中一定含有Ag、Cu,锌不能确定;
(3)在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,若镁粉足量,则铜和铁被全部置换出来,溶液中只含有MgCl2;若镁粉的量不足,只能置换出铜,则溶液中含有FeCl2、MgCl2;若镁粉的量很少,只能置换出部分的铜,则溶液中含有FeCl2、MgCl2、CuCl2,由分析可知,一定含有的溶质是MgCl2.
故答案为:(1)Fe+CuSO4═FeSO4+Cu;(2)Ag、Cu;(3).MgCl2.
点评 本题主要考查了学生对金属活动顺序表的运用以及半待定量(如一定量、过量、少量等)概念的理解和掌握.


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案科目:初中化学 来源: 题型:选择题
| A. | 滤液中一定含有FeSO4,可能含有H2SO4 | |
| B. | 滤液中可能有CuSO4 | |
| C. | 滤渣里一定有Cu,可能有Fe和CuO | |
| D. | 滤渣里一定有Cu和Fe |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
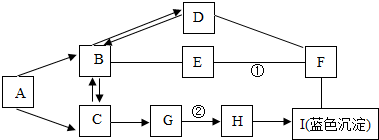 A-I是初中化学所学的物质,其转换关系如图所示.按单质、氧化物、酸、碱、盐分类,A、B、D、E、F是不同类别的物质,C、G、H、I、F也是不同类别的物质;A、B、C中含有同种元素,B是导致“温室效应”的一种气体.图中“一”表示两端的物质能发生化学反应,“→”表示物质间存在相应的转化关系(部分反应物、生成物和反应条件未标出).请回答:
A-I是初中化学所学的物质,其转换关系如图所示.按单质、氧化物、酸、碱、盐分类,A、B、D、E、F是不同类别的物质,C、G、H、I、F也是不同类别的物质;A、B、C中含有同种元素,B是导致“温室效应”的一种气体.图中“一”表示两端的物质能发生化学反应,“→”表示物质间存在相应的转化关系(部分反应物、生成物和反应条件未标出).请回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 反应吸热,降低了可燃物的着火点 | |
| B. | 生成氧化铝覆盖在可燃物表面,隔绝空气 | |
| C. | 生成大量水蒸气,降低可燃物周围氧气的浓度 | |
| D. | 反应能够降低温度,可燃物不易达到着火点 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
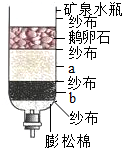 如图是某同学所画的自制简易净水器示意图.
如图是某同学所画的自制简易净水器示意图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com