
����Ŀ����ѧʵ������ȡ����IJ���װ����ͼ��ʾ����ش��������⡣
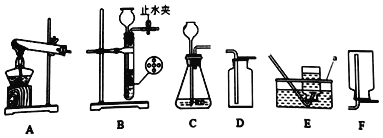
��1������a������_____��
��2��ʵ������ȡ������̼�Ļ�ѧ����ʽΪ_____����Dװ���ռ������壬��������Ϊ_____��
��3����ȡ����ǰҪ����װ�õ������ԣ�����Bװ�������Եķ���Ϊ_____��
��4��ʵ������ȡ�����Ļ�ѧ����ʽΪ_____�����Ʊ����ռ��Ƚϴ�������������ѡ�õ�װ����_____������ĸ����
��5��ʵ������H2O2��MnO2��ȡ������ԭ��Ϊ2H2O2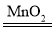 2H2O+O2��������㣺
2H2O+O2��������㣺
��H2O2����Է���������_____��
�����ռ�0.5L������ʵ���������������ܶ�Ϊ1.43gL��1������������_____g��
����ȡ����������Ҫ������������Ϊ5%��˫��ˮ��Һ_____g����ȷ��0.1g����
���𰸡�ˮ�� CaCO3+2HCl��CaCl2+H2O+CO2�� ��ȼ�ŵ�ľ�����ڼ���ƿ�ڣ���ľ��Ϩ��֤��������̼���� �ر�ֹˮ�У�Ȼ��ӳ���©����ע��ˮ��������©�����¶˱�ˮ��û����������ˮ��������©���ڵ�Һ�治���½���˵��װ�õ������������õ� Zn+H2SO4��ZnSO4+H2�� BE��CE 34 0.715 30.4
��������
��1������a��ˮ�ۣ����ˮ�ۣ�
��2��ʵ��������ȡ������̼�ķ���ʽΪ![]() ��������̼��ȼ�ա�Ҳ��֧��ȼ�գ������������ſ��������ռ�������̼ʱ����������Ϊ��ȼ�ŵ�ľ�����ڼ���ƿ�ڣ���ľ��Ϩ��֤��������̼���������
��������̼��ȼ�ա�Ҳ��֧��ȼ�գ������������ſ��������ռ�������̼ʱ����������Ϊ��ȼ�ŵ�ľ�����ڼ���ƿ�ڣ���ľ��Ϩ��֤��������̼���������![]() ����ȼ�ŵ�ľ�����ڼ���ƿ�ڣ���ľ��Ϩ��֤��������̼������
����ȼ�ŵ�ľ�����ڼ���ƿ�ڣ���ľ��Ϩ��֤��������̼������
��3����ȡ����ǰҪ����װ�õ������ԣ�����Bװ�������Եķ���Ϊ�ر�ֹˮ�У�Ȼ��ӳ���©����ע��ˮ��������©�����¶˱�ˮ��û����������ˮ��������©���ڵ�Һ�治���½���˵��װ�õ������������õģ�����ر�ֹˮ�У�Ȼ��ӳ���©����ע��ˮ��������©�����¶˱�ˮ��û����������ˮ��������©���ڵ�Һ�治���½���˵��װ�õ������������õģ�
��4����ʵ�����У�����п����ϡ���ᷴӦ����ȡ������ͬʱ��������п���÷�Ӧ���ڹ�Һ�����ͣ�ѡ��װ��B��C����ȡ������������ˮ��������ˮ�����ռ���Ϊ���������������![]() ��BE��CE��
��BE��CE��
��5����H2O2����Է���������1��2+16��2��34�����34��
��0.5L������������0.5L��1.43gL��1��0.715g�����0.715��
������Ҫ�������������Ϊx
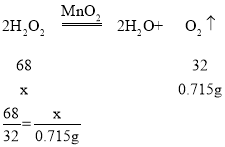
x��1.52g
��ȡ����������Ҫ������������Ϊ5%��˫��ˮ��Һ������Ϊ��1.52g��5%��30.4g
���30.4��


 ��һ������ĩ�ٷֳ�̾�ϵ�д�
��һ������ĩ�ٷֳ�̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ����Ҫ�ġ�����Ԫ�ء����ں�ˮ���κ����ο��й㷺���ڡ�
(1)±ˮ�㶹��ʱ���õ��Ȼ�þ���Ȼ�þ�Ļ�ѧʽΪ_____��
(2)�����Ȼ��ƵĻ����������ӣ�������ӵĻ�ѧ����Ϊ_____����ԭ�ӵĽṹʾ��ͼΪ_____��
(3)��������(NaClO)��Һ����SO2�Ļ�ѧ����ʽΪ:NaClO+SO2+H2O=NaCl+X����X�Ļ�ѧʽΪ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС��������ͼװ��̽���¶ȶ�CO��ԭFe2O3��Ӱ�죨�̶�װ���ԣ���
�������ϣ�CO2+Zn![]() CO+ZnO��FeCl3��Һ��KSCN��Һ��죮
CO+ZnO��FeCl3��Һ��KSCN��Һ��죮
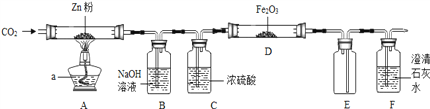
��ش��������⣺
���о�С���Ϊ���飬����ͼװ�ý��жԱ�ʵ�飬�����þƾ��ơ������þƾ���ƶ�װ��D���м��ȣ�������Ϊ��ɫ��ĩ�������������ֱ��ò����������ʵ�飺
���� | ���� | �������� | �������� |
1 | ȡ��ɫ��ĩ�������� | �ܽ⣬�����ݣ���Һ��dz����ɫ�������ֽ������ӣ� | �ܽ⣬�����ݣ���Һ��dz��ɫ |
2 | ȡ����1������Һ���μ�KSCN��Һ | ��� | ������ |
��1��������װ��D�������з�Ӧ�Ļ�ѧ����ʽ��_________________________________������õ��ĺ�ɫ��ĩ��______��
��2���Ӱ�ȫ���ǣ���ʵ��Ӧ��װ��_____��______֮��������װ��E��ֹ������������ĸ��ţ�
��3���öԱ�ʵ��������CO�Ļ�ԭ�������¶ȵ����߶�________�����ǿ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾij����ѧ��Ӧ���йظ÷�Ӧ��˵����ȷ���ǣ�������
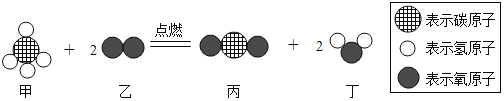
A. ��Ӧǰ����Ԫ�صĻ��ϼ۷����˱仯
B. �÷�Ӧ�����û���Ӧ
C. ���Ĵ����ŷ�������������Ҫԭ��
D. ���ɱ��Ͷ���������Ϊ1��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ɼ�����Ҫ�ɷ��к���̼�����ƣ�ij��ѧ��ȤС���̼�����ƵĻ�ѧ���ʽ�����̽����
ʵ��һ��̽��̼��������Һ������ԣ���pH��ֽ���̼��������Һ��pHԼΪ10���ɴ˿�֪̼��������Һ��______�ԡ�
ʵ�����̽��̼��������Һ�ܷ����ᷴӦ��ȡ������������Թ��У��μ�������ϡ���ᣬ����Ϊ______�����ۣ�̼�����������ᷴӦ��
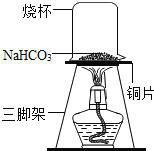
ʵ������̽��̼�����Ƶ����ȶ��ԣ�ȡһ������̼�����Ʒ���ͭƬ�ϼ��ȣ���ͼ��ʾ��
��1������һ��ʱ��۲쵽�ձ��ڱ���ˮ�顣
��2����ּ��Ⱥ��ձ�Ѹ�ٵ�ת���������������ij���ʯ��ˮ�����۲쵽ʯ��ˮ����ǡ�д��ʯ��ˮ����ǵĻ�ѧ����ʽ______��
��3����ͨ����һ��ʵ��̽����ȷ����ּ��Ⱥ�Ĺ������ijɷ֡�
��������裩�ٿ�����Na2CO3�ڿ�����NaOH
�����ʵ�飩
����һ��ȡ������ּ��Ⱥ�Ĺ������Թ��У���������ˮ����ܽ⣬�����Թ��м�������������������Һ���۲쵽��ɫ���������������ٳ�������д��������Ӧ�Ļ�ѧ����ʽ______��
������������ѡ���뷽��һ�в�ͬ�����Լ������һ������
ʵ����� | ʵ������ | ���� |
______ | ______ | ����ٳ���������ڲ����� |
��ʵ����ۣ���д��NaHCO3���ȷֽ�Ļ�ѧ����ʽ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Һ�������Ϳ����о��й㷺����;�������ǵ������ܲ��ɷ֡�
��1���·���մ�е����ۣ���������ϴȥ������Ϊ������_____ ����ܽ⡱���黯�������ۡ�
��2�����˱�����ˮ�Ժ�������á���������˵��������ܽ����_____�йء�
��3��ij�������ʵ��ܽ��������ͼ��ʾ��
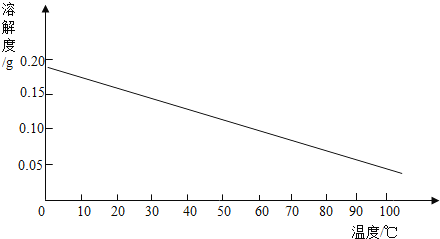
20��ʱ��Ҫʹ�ӽ����͵ĸ����ʵ���Һ��Ϊ������Һ��ͨ���ɲ������ַ��������Ƿֱ���_____��_____��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ��һ�����ù㷺��ũҩ������ʯ�Һ�����ͭ���ƶ��ɡ�ij���������·�Ӧ��2Cu+O2+2H2SO4=2CuSO4+2H2O����������ͭ����Ҫ�Ƶ�80kg ����ͭ���Լ��㣺
��1������ͭ��_______������ţ�Ԫ�ص�����������С��
��2����ǡ������ϡ�����������400kg�����ϡ�������ʵ����������Ƕ��٣�
��3�����������У���������ͭ��Һ�����ʵ����������Ƕ��٣�����������ȷ��0.1%��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͭ��ϡ���ᷢ����Ӧʱ,��������Һ��������ʱ��ı仯������ͼ��ʾ������˵���������
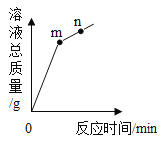
A. ��ʵ���ǽ�ϡ�������뵽ʢ������ͭ��������
B. m���ʾ����ͭ��ϡ����ǡ����ȫ��Ӧ
C. m���n���Ӧ��Һ��ͭԪ�ص����������
D. m���n���Ӧ��Һ�����ᾧ��õ��Ĺ���ɷ���ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȼ��ˮ�������ԣ����ú�ˮ�����Ǽ���SO2�ŷŵ���Ч�������乤����������ͼ��ʾ��
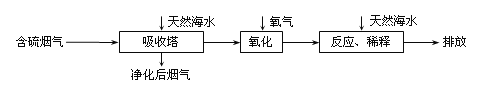
�����˽϶�ĺ�����������H2SO3���ɣ�ͨ�������������Ϸ�Ӧ��ˮ������������ǿ��
�����һ�ּ��龻������������Ƿ�SO2�ļ�ʵ�鷽����____��
���û�ѧ����ʽ��ʾ��ˮ������ǿ��ԭ��____��
��������ĺ�ˮ��Ҫ�ô�������Ȼ��ˮ��֮��Ϻ�����ŷţ��ò�������ҪĿ����____��
��ijͬѧȡһ����������Ʒ�����뺬Ca(OH)2 7.4%��ʯ�ҽ��������е�SO2��ǡ����ȫ����ʱ����ʯ�ҽ�10.00g�����������Ʒ���ܽ�SO2������Ϊ___�ˣ���д��������̣�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com