
分析 (1)根据高锰酸钾化学式的含义进行分析解答.
(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(3)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(4)根据1个高锰酸钾分子的构成进行分析解答.
(5)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
(6)高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,由质量守恒定律,试管内减少的质量即为生成氧气的质量,据此进行分析解答.
解答 解:(1)高锰酸钾是由钾、锰、氧三种元素组成的.
(2)高锰酸钾的相对分子质量为39+55+16×4=158.
(3)高锰酸钾中钾、锰、氧三种元素的质量比39:55:(16×4)=39:55:64.
(4)1个高锰酸钾分子是由1个钾原子、1个锰原子和4个氧原子构成的,则高锰酸钾中锰、钾、氧原子的个数比1:1:4.
(5)高锰酸钾中氧元素的质量分数是$\frac{16×4}{158}$×100%≈40.5%.
(6)由质量守恒定律,生成氧气的质量为4.8g+1.0g-5.48g=0.42g.
设被分解高锰酸钾的质量为x.
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
x 0.42g
$\frac{316}{32}$=$\frac{x}{0.42g}$ x≈4.15g.
被分解高锰酸钾的质量是$\frac{4.15g}{4.8g}×$100%≈86.5%.
故答案为:(1)三;(2)158;(3)39:55:64;(4)1:1:4;(5)40.5%;(6)被分解高锰酸钾的质量是86.5%.
点评 本题难度不大,掌握化学式的含义与有关计算、化学方程式的有关计算等是正确解答本题的关键.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
 硫酸钠在不同温度时的溶解度数据如表:
硫酸钠在不同温度时的溶解度数据如表:| 温度/℃ | 0 | 10 | 20 | 30 | 40 |
| 溶解度/g | 4.5 | 9.5 | 20.5 | 40.8 | 48.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
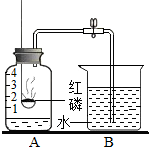 某同学用如图装置是测定空气中氧气含量的实验,先把A中水面以上分成五等份由下至上刻度分为1、2、3、4.请你填写有关空格.
某同学用如图装置是测定空气中氧气含量的实验,先把A中水面以上分成五等份由下至上刻度分为1、2、3、4.请你填写有关空格.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 现象 | 结果分析 |
| 1.取少量甲组废液于试管中,静置观察 | 试管底部有白色沉淀,上层为无色澄清液 | 白色沉淀为(填化学式,下同)(1)BaCO3 |
| 2.取上层无色澄清液,滴加紫色石蕊试剂 | 溶液仍然为紫色 | 澄清液的溶质中一定含有NaCl和(2)NaNO3 ,可能含有物质A是(3)Ba(NO3)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 目的 | 区分食盐水和稀盐酸 | 区分羊毛绒和棉线 | 区分硝酸铵粉末和氧化钙粉末 | 区分聚乙烯和聚氯乙烯 |
| 方案 | 滴加硝酸银溶液 | 灼烧闻气味 | 加水 | 灼烧闻气味 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某同学在实验室里用下列装置进行实验,请回答下列问题:
某同学在实验室里用下列装置进行实验,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com