
分析 (1)方案一:根据氢氧化钠和碳酸钠溶液都呈碱性进行解答;
方案二:根据盐酸要先与氢氧化钠反应进行解答;
方案三:根据碳酸钠能和氯化钡溶液、氯化钙溶液、硝酸钙溶液等反应产生白色沉淀进行解答;
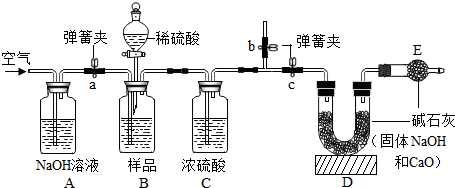
(2)①根据空气中含有二氧化碳,氢氧化钠溶液能吸收二氧化碳进行解答;
②根据通入空气的目的是排出装置中的CO2进行解答;
③根据浓硫酸具有吸水性,能除去二氧化碳气体中的水蒸气进行解答;
④根据E中碱石灰的作用是防止空气中的水和二氧化碳进入D装置进行解答;
⑤根据D装置增重2.2克是生成二氧化碳的质量进行解答;
⑥根据氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠进行解答.
解答 解:(1)方案一:氢氧化钠和碳酸钠溶液都呈碱性,所以不能用酚酞试液检验是否含有碳酸钠;故填:两种溶液都呈碱性;
方案二:盐酸要先与氢氧化钠反应生成氯化钠和水,所以配成溶液,向其中慢慢滴加稀盐酸,大家发现刚开始滴加时无气泡产生,化学方程式为NaOH+HCl=NaCl+H2O;故填:NaOH+HCl=NaCl+H2O;
方案三:碳酸钠能和氯化钡溶液、氯化钙溶液、硝酸钙溶液等反应产生白色沉淀,所以配成溶液,向其中滴加BaCl2、CaCl2、Ca(NO3)2 等的溶液,可以证明含有碳酸钠;故填:BaCl2、(或CaCl2、Ca(NO3)2 等);
(2)①空气中含有二氧化碳,氢氧化钠溶液能吸收二氧化碳,所以装置A的作用是除去空气中的CO2;故填:除去空气中的CO2;
②通入空气的目的是排出装置中的CO2;若不再通入空气,装置中有剩余二氧化碳,使得计算出的碳酸钠的质量较小,则测得工业烧碱的纯度将偏高;故填:排出装置中的CO2;偏高;
③浓硫酸具有吸水性,能除去二氧化碳气体中的水蒸气,所以若撤去C装置,使得计算出的碳酸钠的质量偏大,则测得工业烧碱的纯度将偏低;故填:偏低;
④E中碱石灰的作用是防止空气中的水和二氧化碳进入D装置;故填:防止空气中的水和二氧化碳进入D装置;
⑤设碳酸钠的质量为x
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 44
x 2.2g
$\frac{106}{x}=\frac{44}{2.2g}$
x=5.3g
样品中烧碱的纯度=$\frac{50g-5.3g}{50g}×100%$=89.4%
答:样品中烧碱的纯度为89.4%
⑥氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,所以可用氢氧化钙溶液除去碳酸钠.故填:Ca(OH)2.
点评 解答这类题目时,首先,赏析问题情景,找到实验探究的反应原理,弄清个装置的作用;再根据实验的反应原理,分析推断出该物质的组成成分,然后得出所要探究的物质中该成分的组成.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如果将物质按单质、氧化物、酸、碱、盐、有机物分类,如图中甲、乙、丙是三种不同类别的物质,且相连物之间均能发生化学反应,下列说法符合图示要求的是( )
如果将物质按单质、氧化物、酸、碱、盐、有机物分类,如图中甲、乙、丙是三种不同类别的物质,且相连物之间均能发生化学反应,下列说法符合图示要求的是( )| A. | 当甲、乙、丙分别为酸、碱、盐时,X一定不可能为碳酸钠 | |
| B. | 当X为氧气时,甲、乙、丙可以为镁、红磷、葡萄糖 | |
| C. | 当X为稀盐酸时,甲、乙、丙可以为铜、氢氧化铜、硝酸银 | |
| D. | 当甲为氯化铵时、乙为硫酸时,丙为氧化铝时,X可以为氢氧化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 稀盐酸 氯化钠溶液 碳酸钠溶液 硝酸钾溶液 | |
| B. | 稀硫酸 稀盐酸 酚酞试液 氢氧化钠溶液 | |
| C. | 稀盐酸 酚酞试液 碳酸钠溶液 氢氧化钠溶液 | |
| D. | 稀盐酸 石灰水 硝酸钡溶液 碳酸钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 正常雨水的pH 约为5.6是因为CO2+H2O=H2CO3 | |
| B. | 医疗上用含有Mg(OH)2的药剂治疗胃酸过多的病症:Mg(OH)2+2HCl═MgCl2+2H2O | |
| C. | 用稀盐酸除铁锈:Fe2O3+6HCl═2FeCl3+3H2O | |
| D. | 用稀盐酸除去试管壁上残留的铜:2HCl+Cu=CuCl2+H2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 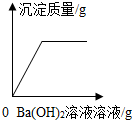 向H2SO4和CuSO4的混合溶液中滴加Ba(OH)2溶液 | |
| B. | 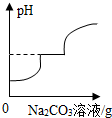 向HCl和CaCl2混合溶液中滴加Na2CO3溶液 | |
| C. | 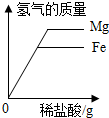 向等质量的Mg和Fe中滴加稀盐酸 | |
| D. | 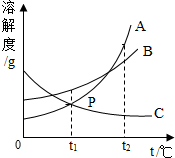 将t2℃时A、B、C的饱和溶液降温至t1℃时,其溶质质量分数大小关系为B>A=C |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com