
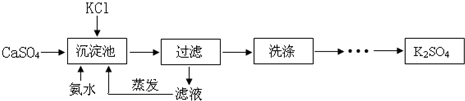
| 温度(℃) | 0 | 10 | 26 | 30 |
| 水溶液 | 7.31 | 9.28 | 11.03 | 12.98 |
| 氨(8%)溶液 | 1.41 | 1.58 | 2.25 | 3.36 |
| 氨(35%)溶液 | 0.44 | 0.75 | 0.82 | 非常压 |
分析 根据物质的酸碱性与pH的关系、氨气在水中的溶解因素、过滤操作需要的仪器以及物质的性质进行分析解答即可.根据题干提供的数据结合硫元素质量守恒计算即可.
解答 解:(1)氨水呈碱性,向水中连续通氨气达两个小时可得高浓度氨水,氨气不断溶解则碱性增强,故会使溶液pH增大;
常压30℃时氨气在水中达到饱和时浓度小于35%,故常压下不能形成30℃的氨(35%)溶液.
(2)根据表格提供的数据可以看出,氨水浓度越大,硫酸钾溶解度越小,故沉淀池中氨水浓度常常控制在25%至40%;沉淀池温度适宜保持在低温;
(3)滤液经蒸发后产生可以循环使用的气体是氨气,其化学式为NH3;根据反应的化学方程式可以看出:
CaCO3+2HNO3═Ca(NO3)2+H2O+CO2↑
溶质硝酸和溶剂水的微粒个数比为:
2HNO3--5H2O
126 90
故硝酸和水的质量比为:126:90=7:5;
(4)实验室进行过滤操作需要的玻璃仪器有烧杯、玻璃棒、漏斗,稀释浓硫酸时用到玻璃棒的主要作用为 使溶解产生的热量及时散发,防止局部过热而引起液体飞溅.
(5)沉淀若是洗涤干净,则不含有氢氧化钙,氢氧化钙呈碱性,能使酚酞变红,能与碳酸钠反应产生沉淀,不能与氯化钡反应,故检验沉淀是否洗净的试剂是AB;
(6)二氧化硫排放到空气中会造成空气污染,随雨水降落会形成酸雨;二氧化硫能使高锰酸钾溶液褪色,可以用高锰酸钾溶液检验二氧化硫;
(7)转化生成石膏的硫元素的质量为:200t×2.5%×96%=4.8t
设生产石膏的质量为x,根据硫元素质量守恒,可以得到:
S------CaSO4•2H2O
32 172
4.8t x
$\frac{32}{172}=\frac{4.8t}{x}$
x=25.8t
故答案为:(1)碱性,增大,常压30℃时氨气在水中达到饱和时浓度小于35%.
(2)氨水浓度越大,硫酸钾溶解度越小,低温.
(3)NH3,7:5;
(4)漏斗;使溶解产生的热量及时散发,防止局部过热而引起液体飞溅;
(5)AB;
(6)形成酸雨;高锰酸钾;
(7)生产石膏25.8t.
点评 本题考查的是常见的物质的制备,难度较大,完成此题,可以依据已有的物质的性质结合题干提供的信息进行.


科目:初中化学 来源: 题型:选择题
| 选项 | 方法 | 示例 |
| A | 观察法 | 变化中观察到有发光、放热现象即可说明发生了化学变化 |
| B | 归纳法 | 根据稀盐酸、稀硫酸等物质的化学性质,归纳出酸的通性 |
| C | 分类法 | 根据组成物质的元素种类,将纯净物分为单质和化合物 |
| D | 实验法 | 用新配制的氢氧化铜悬浊液可检验葡萄糖 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | X>Y>Z | B. | Y>X>Z | C. | Z>X>Y | D. | Y>Z>X |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
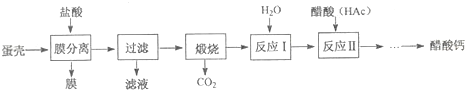
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
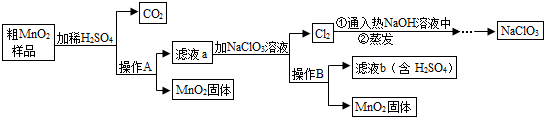
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
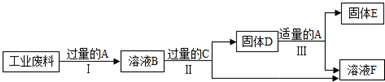
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 苯不属于有机物 | |
| B. | 苯是由6个碳原子和6个氢原子构成的 | |
| C. | 可通过加热蒸发的方法除去水中的苯 | |
| D. | 常温下可通过滤纸过滤的方法除去水中的苯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com