
【题目】金属与生活息息相关,认识金属的性质对我们至关重要,认真阅读材料一和二,回答问题。
材料一:镓(Ga)是灰蓝色或银白色的金属,熔点很低,沸点很高,其化学性质与铝相似,能与氧气在加热时反应。金属镓广泛应用于半导体材料,光电子工业和微波通讯工业等领域。(提示:镓元素在化合物中的化合价为+3价)
(1)镓的物理性质:_____。
(2)写出镓与氧气反应的化学方程式_____。
材料二:2018年10月28日,国人为之骄傲的第一艘001A型国产航母第三次海试,标志着我国在航海及军事领域取得重大突破。
(3)合金是航母的主体材料,如铝合金等,其中,_____和它的合金被称为21世纪最为重要的金属材料,医疗中常用于人造骨头和关节材料。
(4)航母的外壳用涂料覆盖是为了防止钢铁材料与空气中_____接触而生锈,请写出种生活中防止钢铁制品生锈的方法_____。
(5)下列制品的用途,利用金属导热性的是_____(填序号)。

【答案】镓(Ga)是灰蓝色或银白色的金属,熔点很低,沸点很高(写出一条即可得分) ![]() Ti(或钛) 氧气和水(或O2、H2O) 刷漆等 A
Ti(或钛) 氧气和水(或O2、H2O) 刷漆等 A
【解析】
(1)镓的物理性质:灰蓝色或银白色的金属,熔点很低,沸点很高;
(2)镓与氧气反应生成氧化镓的化学方程式:![]() ;
;
(3)合金是航母的主体材料,如铝合金等,其中,钛和它的合金被称为21世纪最为重要的金属材料,医疗中常用于人造骨头和关节材料。
(4)钢铁在潮湿的空气中容易生锈,航母的外壳用涂料覆盖是为了防止钢铁材料与空气中氧气和水接触而生锈,生活中防止钢铁制品生锈的方法:刷漆、涂油等
(5)下列制品的用途,利用金属导热性的是:
A 铁锅,利用金属导热性;故选项正确;
B 导线,利用金属导电性;故选项错误;
C 钢丝绳,利用金属的延展性;故选项错误;
D 黄金饰品,利用金属的稳定性;故选项错误;
故选:A。


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:初中化学 来源: 题型:
【题目】下列实验方法能达到实验目的的是( )
选项 | 实验目的 | 实验方法 |
A | 除去 | 加入足量锌粉 |
B | 检验一瓶气体是否为 | 将燃着的木条伸入瓶中 |
C | 检验蜡烛燃烧的产物中是否有水 | 在火焰上方罩一只冷而干燥的烧杯 |
D | 分离铜粉和铁粉 | 加水,过滤 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具,是国际通用的化学语言.
(1)请用化学用语填空:
①地壳中含量最多的元素 ;②两个氢原子 ;
③三个二氧化硫分子 ;④四个氢氧根离子 .
(2)在符号“![]() O”中H正上方的“+1”表示 ,H右下角的“2”表示 .
O”中H正上方的“+1”表示 ,H右下角的“2”表示 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在学习过程中,小雨同学提出一个问题:“碳燃烧时可能生成CO2,也可能生成CO,那么碳与氧化铜反应生成的气体也有多种可能吗?”
(猜想)碳与氧化铜反应生成的气体中:①只有CO2;②只有CO;③_____________。
(查阅资料)浸有磷钼酸溶液的氯化钯试纸遇CO2,无变化,但遇到微量CO会立即变成蓝色。
(方案设计)通过上述资料和已有知识,小雨初步设想用浸有磷钼酸溶液的氯化钯试纸和澄清石灰水对碳与氧化铜反应生成的气体进行检验。根据小雨的设想,请你完成填空。
(1)若试纸不变色,澄清石灰水变浑浊,则猜想①成立。
(2)若试纸______,澄清石灰水_______,则猜想②成立。
(3)若试纸______,澄清石灰水_______,则猜想③成立。
(实验验证)经过思考之后,小雨设计了如下图所示的实验装置。
实验步骤:
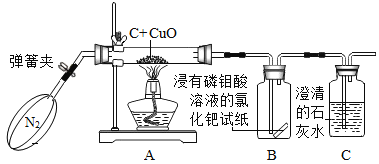
(1)打开弹簧夹,先通一会儿纯净、干燥的N2。
(2)关闭弹簧夹,点燃酒精灯加热。
(结论)小雨通过分析实验现象,确认猜想③是正确的。请你写出装置A中发生反应的化学方程式_______________;_____________;
(反思与评价)该实验开始通一会儿N2的目的是_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】类比法是化学研究物质的重要方法之一,草酸的化学性质与碳酸相似。已知碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物。某校研究性学习小组对此展开探究:
(1)小明首先根据草酸中含有_________元素,可推测生成物中含有水。
(2)小明对分解生成的其他产物进行推测、验证。
(假设一)生成物中有二氧化碳。
实验一:将生成的气体通入澄清石灰水中,实验现象是___________,请写出该反应的化学方程式___________。小明据此判断生成物中含有二氧化碳。
(假设二)生成物中有一氧化碳。
实验二:小明用下图装置进行实验,从而证明生成物中含有一氧化碳。

请回答:A装置中的实验现象是_______________。
(3)小芳认为,小明的“实验二”不需要B装置也能够推断出生成物中含有一氧化碳,你是否支持小芳的观点:________________(填“支持”或“不支持”),请说出你的理由:________________。
(4)小红认为,从环保的角度看,“实验二”装置有一个缺陷,请你指出该缺陷:_____________,处理的两种方法是:_____________、_______________。
(5)为避免有毒的CO污染空气,所以含碳元素的物质燃烧必须满足的条件是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下面部分金属的活动性顺序回答:
![]()
(1)上述金属中活动性最强的是 ;
(2)按年代最早被广泛使用的金属是 ;
(3)已知:①X+H2SO4=XSO4+H2↑ ②Y+2ZNO3=Y(NO3)2+2Z ③Y与稀硫酸不反应。则符合要求的X、Y、Z分别是 (填字母序号)。
A.Cu、Hg、Ag B.Fe、Cu、Ag C.Mg、Zn、Fe
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】自然界中存在一种非常漂亮的孔雀石,其主要成分是碱式碳酸铜,俗称铜绿,化学式为[Cu2(OH)2CO3],受热可分解生成氧化铜、水和二氧化碳。
(1)孔雀石多在原始森林中,人类很早就发现,孔雀石在熊熊燃烧的树木中灼烧后,余烬里有一种红色光亮的金属显露出来,请用两个主要的反应方程式说明这种变化_____;_____。
(2)铜绿分解生成44g二氧化碳的同时,生成CuO的质量_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酸和碱作用生成盐和水的反应叫中和反应。某化学兴趣小组同学对“盐酸中和氢氧化钠溶液”的反应进行探究。
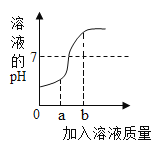
(1)小明在做“盐酸中和氢氧化钠溶液”的实验时,测出反应过程中溶液的pH变化如图所示。
①该反应的化学方程式为:___________________。
②该实验操作是将_________________滴加到另一种溶液中。
③当加入溶液的质量为ag时,所得溶液中的阳离子有(写符号)_______________。
④当加入溶液的质量为bg时,向所得溶液溶液中滴入紫色石蕊试液,紫色石蕊试液变_______色。
(2)小亮在做“盐酸中和氢氧化钠溶液”的实验时,向氢氧化钠溶液里滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度,于是他对所得溶液的酸碱性进行探究。
(探究目的)探究所得溶液的酸碱性。
(提出猜想)所得溶液可能呈酸性,也可能呈____________性,还可能呈碱性。
(实验验证)
实验操作 | 实验现象 | 结论 |
用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡。 | 无色酚酞试液变________色 | 溶液呈碱性 |
无色酚酞试液不变色 | 溶液呈_________。 |
(交流与反思)
①若溶液呈碱性,则溶液中使其呈碱性的离子是_________(写符号)。
②若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入镁条,若有____________现象,则呈酸性;若无明显现象,则呈中性。
方案二:取样,加入一枚表面生锈的铁钉,若观察到铁锈消失、溶液变成黄色,则所取溶液呈酸性,反应的化学方程式为____________;若无明显现象,则呈中性。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在研究酸和碱的化学性质时,某小组想证明稀硫酸和氢氧化钠混合后,虽然无明显现象,但确实发生了化学反应。试与他们一起完成实验方案的设计、实施和评价,并得出有关结论。
(1)探究稀硫酸和氢氧化钠溶液的反应:
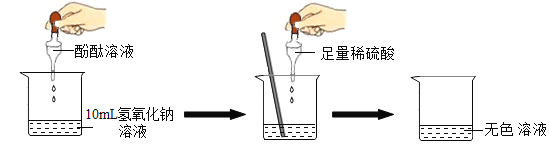
当滴入几滴酚酞溶液后,溶液由无色变为_________色。根据上述实验中颜色变化,可确定稀硫酸和氢氧化钠溶液发生了化学反应。
(2)探究上述稀硫酸和氢氧化钠溶液反应后烧杯中的硫酸是否过量:根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量。同学们又分别选取氯化钡溶液、紫色石蕊溶液设计实验方案,请你判断并(提示:Ba2+与SO42-可形成BaSO4白色沉淀)
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的氯化钡溶液 | 有白色沉淀生成 | 稀硫酸过量 |
方案二 | 取样,滴入几滴紫色石蕊溶液 | _________ | 稀硫酸过量 |
①上述设计的实验方案中,正确的方案是:__________。
②若请你再设计一个确定稀硫酸是否过量的实验方案,你会选用的药品是_______,实验现象及结论是_____________。
(3)成成同学认为稀硫酸和氢氧化钠溶液的反应没有明显现象,他提出可以对某些有明显现象产生的中和反应进行探究,如稀盐酸和氢氧化铝的反应,可观察到的现象为_________,说明中和反应已经发生,反应的化学方程式为_______________。。(提示:氢氧化铝是不溶于水的白色固体,化学式为Al(OH)3)。
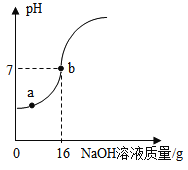
(4)现取10g一定溶质质量分数的稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化情况如图所示。计算恰好完全反应时所得溶液的溶质质量分数______。(结果精确到0.1%)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com