
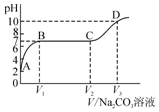
 小明测得石灰石与一定量的稀盐酸反应后的溶液pH为2,取适量该溶液向其中逐滴加入碳酸钠溶液,并测得溶液pH随加入碳酸钠溶液体积的变化曲线如图所示.则下列有关说法不正确的是( )
小明测得石灰石与一定量的稀盐酸反应后的溶液pH为2,取适量该溶液向其中逐滴加入碳酸钠溶液,并测得溶液pH随加入碳酸钠溶液体积的变化曲线如图所示.则下列有关说法不正确的是( )| A. | A点处溶液中的溶质是CaCl2 | |
| B. | AB段可观察到的实验现象是有气泡产生 | |
| C. | BC段发生反应的产物是CaCO3、NaCl | |
| D. | CD段pH上升的原因是Na2CO3过量 |
分析 测得石灰石与一定量的稀盐酸反应后的溶液pH为2,说明反应后的溶液中的溶质是反应生成的氯化钙和过量的氯化氢,向其中逐滴加入碳酸钠溶液时,碳酸钠先和氯化氢反应生成氯化钠、水和二氧化碳,随着反应进行,溶液酸性减弱,pH升高,当氯化氢完全反应后溶液显中性,pH等于7,继续加入碳酸钠溶液时,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,溶液酸碱性不变,当氯化钙完全反应后,继续加入碳酸钠溶液时,溶液显碱性,pH升高.
解答 解:A、A点是加入碳酸钠溶液前,此处溶液中的溶质是反应生成的氯化钙和过量的氯化氢,该选项说法不正确;
B、AB段是碳酸钠和稀盐酸反应,能够生成二氧化碳气体,因此可观察到的实验现象是有气泡产生,该选项说法正确;
C、BC段发生反应是碳酸钠和氯化钙反应生成碳酸钙和氯化钠,该选项说法正确;
D、碳酸钠溶液显碱性,CD段pH上升的原因是Na2CO3过量,该选项说法正确.
故选:A.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


科目:初中化学 来源: 题型:选择题
| 物质 | A | B | C | D |
| 反应前的质量(g) | 6.4 | 3.2 | 4.0 | 2.5 |
| 反应后的质量(g) | 3.8 | 待测数据 | 7.2 | 2.5 |
| A. | A和B是反应物,D可能是催化剂 | |
| B. | 上表中的待测数据的数值为2.6 | |
| C. | C物质中元素的种类,一定等于A、B二种物质中元素的种类之和 | |
| D. | 该反应一定属于分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 现象 | 结论 |
| 取少量废液缸中上层清液,向其中加入一定量的③H2SO4溶液.(填化学式,限填一种) | 无明显现象 | 猜想I正确 |
| ④有白色沉淀产生 | 猜想II正确 | |
| 有气泡产生 | 猜想III正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
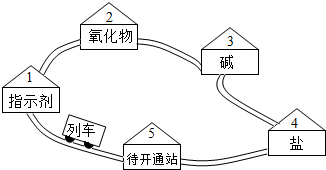 请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站.“2-5号站”各站的对应物质属于不同类别的纯净物.
请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站.“2-5号站”各站的对应物质属于不同类别的纯净物.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①③⑤ | C. | ②④⑤ | D. | ①③④⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
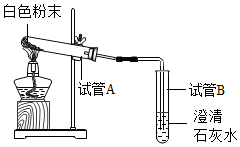 兴趣小组获得两包制作“跳跳糖”的添加剂,一包是柠檬酸晶体,另一包是标注为钠盐的白色粉末.将少量柠檬酸和这种白色粉未溶于水,混合后产产生了使澄清石灰水变浑浊的气体.于是对白色粉末的化学成分进行了以下探究:
兴趣小组获得两包制作“跳跳糖”的添加剂,一包是柠檬酸晶体,另一包是标注为钠盐的白色粉末.将少量柠檬酸和这种白色粉未溶于水,混合后产产生了使澄清石灰水变浑浊的气体.于是对白色粉末的化学成分进行了以下探究:| 实验操作 | 实验现象 | 实验结论 | |
| 小月 | 将白色粉末溶于水后用pH试纸测定其酸碱度 | pH>7(填“>”、“<”或“=”) | 溶液呈碱性,猜想1成立 |
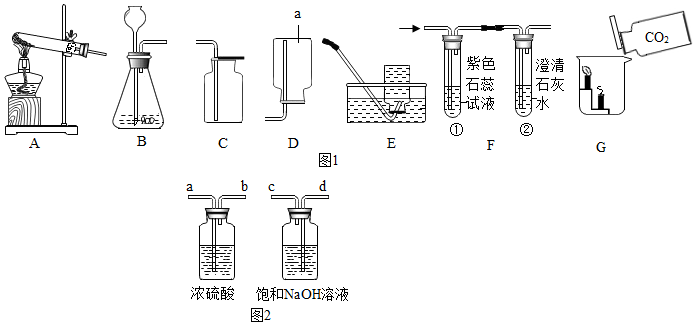
| 小妮 | 用如图所示的装置进行实验 | 试管A中有水珠产生,试管B中液体变浑浊 | 猜想2成立,试管B中反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na+、Fe3+、NO3-、Cl- | B. | Ba2+、NH4+、SO42-、OH- | ||
| C. | Ag+、H+、Cl-、NO3- | D. | H+、Na+、NO3-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com