
��7�֣��ڻ̽�����ϣ���ʦ����һ�����Ȼ��ơ�̼���ơ�̼����������������ȡ�����������ʵ�������϶��ɵİ�ɫ��ĩ��һƿû�б�ǩ��δ֪����Һ�����ʵ��С��ͬѧ���гɷ�ȷ������С��ͬѧ���Ŀα������������ʵ�鷽����

|
�����Dz�֪��AΪ�˵���������������벻���ٵ����ʣ�B��ʹ����ʯ��ˮ����ǡ� ��ش��������⣺
��1��д���������ƣ�B ��δ֪����Һ ��
��2�������ɫ��ĩ����ɿ����� ���йط�Ӧ�Ļ�ѧ����ʽΪ ��
��3������С���ͬѧȡ10g��ɫ��ĩҲ���ռ���ͬѧ�ķ�������ʵ�飬�������յõ����������Ϊ8.5g������Ϊ�����ɫ��ĩ����ɿ����� ��
��1��������̼ ����
��2��NaCl��Na2CO3��NaCl��NaHCO3��Na2CO3��NaHCO3
Na2CO3 + 2HCl = 2NaCl + H2O + CO2����NaHCO3 + HCl= NaCl + H2O + CO2��
��3��NaCl��NaHCO3 Na2CO3��NaHCO3
��������
�����������1��������ɫ����B��ʹ����ʯ��ˮ����ǣ���B�Ƕ�����̼����AΪ�˵���������������벻���ٵ����ʣ��Ҹ���ͼʾ��֪����ɫ��ĩ���Ȼ��ơ�̼���ơ�̼���������������е��������ʣ���ij�ᷴӦ����A��Һ�Ͷ�����̼���壬���������غ㶨�ɣ�Ԫ������䣩��֪��A������Ԫ�أ��Ӷ���ȷ��AΪ�Ȼ��ƣ�������ɫ��Һ���Ȼ�����Һ����δ֪����Һ�к��������ӣ�����ƶ�δ֪����ҺΪϡ���ᡣ
��2����Ϊ��ɫ��ĩ���Ȼ��ơ�̼���ơ�̼���������������е��������ʣ���ϡ���ᷴӦ�ж�����̼���ɣ��ɴ˿��ƶϰ�ɫ��ĩ�к���̼������ӻ�̼��������ӣ������ڰ�ɫ��ĩ��ϡ���ᷴӦ�����Ȼ�����Һ����˸ð�ɫ��ĩ���ܵ����Ϊ��NaCl��Na2CO3��NaCl��NaHCO3��Na2CO3��NaHCO3���ʷ�Ӧ�Ļ�ѧ����ʽ�ֱ�ΪNa2CO3+2HCl=2NaCl+H2O+CO2����NaHCO3+HCl=NaCl+H2O+CO2����
��4��8.5gNaCl����Ԫ�ص�����=8.5g��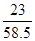 ��100%=3.34g�����ݻ�ѧ�仯ǰ����Ԫ���������䣬��10g��ɫ�����������ķ���=
��100%=3.34g�����ݻ�ѧ�仯ǰ����Ԫ���������䣬��10g��ɫ�����������ķ���=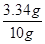 ��100%=33.4%��
��100%=33.4%��
��NaCl����Ԫ����������=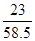 ��100%=39.3%��
��100%=39.3%��
Na2CO3����Ԫ����������=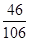 ��100%=43.3%��
��100%=43.3%��
NaHCO3����Ԫ����������=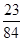 ��100%=27.4%��
��100%=27.4%��
��Ϊ39.3%��33.4%��27.4%������ɫ��ĩ�����ΪNaHCO3��NaCl��
��Ϊ43.3%��33.4%��27.4%������ɫ��ĩ�����Ҳ����ΪNa2CO3��NaHCO3
���㣺֤��̼���Σ�CO32-���鷽���������ʵļ����ƶϣ���д��ѧ����ʽ
�����������漰���ʵ��ƶϣ��ƶ����漰��֪ʶ��࣬�仯���ӣ��������Σ���һ�ּȿ���֪ʶ���ֿ������������ͣ�����Ĺؼ���������Ļ������������ͻ�ƿڣ��������������ʻ�Ӧ����ȣ��ٸ������е�����������Ŀ�ļ��裬Ȼ�����ż�������Ƶ���ֻҪ���������㣬����ͳ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010�챱����ͨ�����п�һģ��ѧ�Ծ����������� ���ͣ��ƶ���
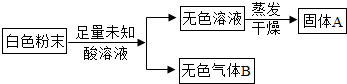
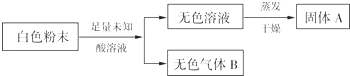
��7�֣��ڻ̽�����ϣ���ʦ����һ�����Ȼ��ơ�̼���ơ�̼����������������ȡ�����������ʵ�������϶��ɵİ�ɫ��ĩ��һƿû�б�ǩ��δ֪����Һ�����ʵ��С��ͬѧ���гɷ�ȷ������С��ͬѧ���Ŀα������������ʵ�鷽����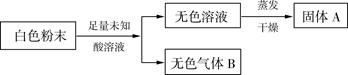
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ڻ̽�����ϣ���ʦ����һ�����Ȼ��ơ�̼���ơ�̼����������������ȡ�����������ʵ�������϶��ɵİ�ɫ��ĩ��һƿû�б�ǩ��δ֪����Һ�����ʵ��С��ͬѧ���гɷ�ȷ������С��ͬѧ���Ŀα������������ʵ�鷽����
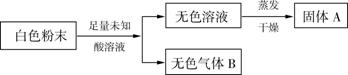
�����Dz�֪��AΪ�˵���������������벻���ٵ����ʣ�B��ʹ����ʯ��ˮ����ǡ�
��ش��������⣺
��1��д���������ƣ�B ��δ֪����Һ ��
��2�������ɫ��ĩ����ɿ����� ���йط�Ӧ�Ļ�ѧ����ʽΪ ��
��3������С���ͬѧȡ10g��ɫ��ĩҲ���ռ���ͬѧ�ķ�������ʵ�飬�������յõ����������Ϊ8.5g������Ϊ�����ɫ��ĩ����ɿ����� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com