
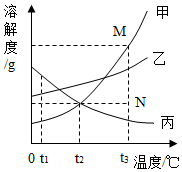
 图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述错误的是( )
图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述错误的是( )| A. | t2℃时,三种物质的溶解度大小顺序为:乙>甲=丙 | |
| B. | t2℃时,甲、丙两种物质的溶液中溶质的质量分数相等 | |
| C. | 若甲物质中混有少量的乙物质,可用降温结晶的方法提纯甲 | |
| D. | 采用降低温度的方法,可将饱和的丙物质溶液变成不饱和 |
分析 根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而丙的溶解度随温度的升高而减少;t2℃时,三种物质的溶解度大小顺序为:乙>甲=丙正确;t2℃时,甲、丙两种物质的溶液中溶质的质量分数相等错误,因为没有指明是饱和溶液;若甲物质中混有少量的乙物质,可用降温结晶的方法提纯甲,因为甲受温度的影响变化比较大;采用降低温度的方法,可将饱和的丙物质溶液变成不饱和,因为丙的溶解度随温度的升高而减少.
解答 解:A、由溶解度曲线可知:t2℃时,三种物质的溶解度大小顺序为:乙>甲=丙正确,正确但不符合题意,故选项错误;
B、t2℃时,甲、丙两种物质的溶液中溶质的质量分数相等错误,因为没有指明是饱和溶液,错误符合题意,故选项正确;
C、若甲物质中混有少量的乙物质,可用降温结晶的方法提纯甲,因为甲受温度的影响变化比较大,正确但不符合题意,故选项错误;
D、采用降低温度的方法,可将饱和的丙物质溶液变成不饱和,因为丙的溶解度随温度的升高而减少,正确但不符合题意,故选项错误;
故选B
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关饱和溶液和不饱和溶液的相互转化,本考点主要出现在选择题和填空题中.


科目:初中化学 来源: 题型:解答题
| 元素名称 | 钠 | 镁 | 铝 | 硅 | 磷 | 硫 | 氯 | 氩 |
| 元素符号 | Na | Mg | Al | Si | P | S | Cl | Ar |
| 原子结构示意图 | 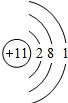 | 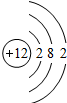 | 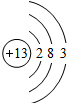 | 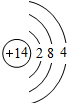 | 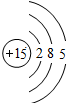 | 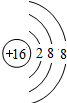 | 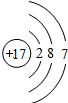 | 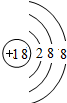 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 待提纯的物质 | 选用的试剂 | 操作的方法 |
| A | CaO(CaCO3) | 水 | 溶解、过滤、结晶 |
| B | Cu(CuO) | 稀盐酸 | 溶解、过滤、洗涤、干燥 |
| C | CuSO4(H2SO4) | 氢氧化钠溶液 | 过滤 |
| D | H2O(CO2) | 浓硫酸 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
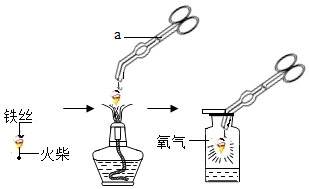 实验是研究化学的基本手段.在实验室,小冬同学进行了“铁在氧气中燃烧”的实验,请回答下列问题:
实验是研究化学的基本手段.在实验室,小冬同学进行了“铁在氧气中燃烧”的实验,请回答下列问题:| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
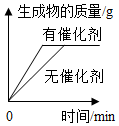 某同学为了探究氧化铜(难溶于水)是否能做过氧化氢(H2O2)分解制取氧气的催化剂,设计实验如下:
某同学为了探究氧化铜(难溶于水)是否能做过氧化氢(H2O2)分解制取氧气的催化剂,设计实验如下:| 1.在试管中加入2ml5%的过氧化氢溶液,将带火星的木条伸入试管中,观察现象. | 1.带火星的木条没有明显变化 |
| 2.取1gCuO粉末放在放在步骤1中的试管中,振荡,把带火星的木条伸入试管中 | 2.带火星的木条复燃 |
| 实验步骤 | 实验现象 |
| 待实验一第2步的试管中没有气泡时,重新加入2ml过氧化氢溶液,观察现象. | 试管中有大量的气泡冒出 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com