
| A. |  | B. | 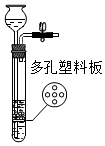 | C. | 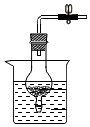 | D. | 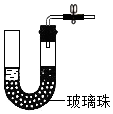 |
分析 根据装置之所以能控制反应的进行与停止,就是因为它当将装置中的导气管关闭后,生成的气体使装置中的气压增大,从而使固体和液体分离,使反应停止解答.
解答 解:
A中可上下移动铜丝,把液体和固体分离,不能通过气压的变化控制反应的发生和停止;
B中有一个隔板,当打开止水夹时固液接触,反应发生;当关闭止水夹时,随着气压的增大,把部分液体压入长颈漏斗,使固液分离,反应停止,因此可以实现使反应随时发生随时停止的目的;
C中可以通过把装置放进烧杯或拿出实现固液的接触或分离,也能关上止水夹,随着气压的增大,使球形管中的液面会下降,从而实现使反应随时发生随时停止的目的;
D中当打开止水夹时固液接触,反应发生;当关闭止水夹时,随着气压的增大,把液体压入U型管的左端,使固液分离,反应停止,因此可以实现使反应随时发生随时停止的目的;
答案:A
点评 解答本题的关键是明确使反应随时发生随时停止的反应原理:固液随时接触随时分离.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | H2O2 | B. | HCl溶液 | C. | NaOH溶液 | D. | AgNO3溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 消耗等质量的H2SO4 | B. | 生成等质量的ZnSO4 | ||
| C. | 消耗等质量的CuO | D. | 所有反应的条件相同 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
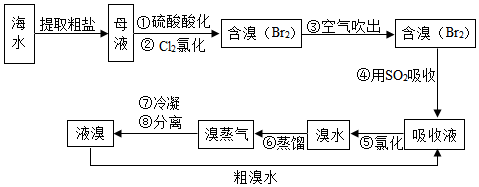
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 5.4g | B. | 6.2g | C. | 7.8g | D. | 9.0g |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
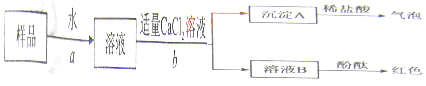
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
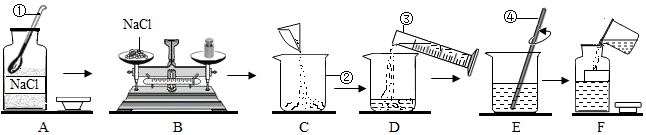
| A. | 称量固体食盐时,所用砝码已生锈 | |
| B. | 称量完固体食盐时,天平指针向左倾斜 | |
| C. | 用量筒取水时,仰视读数 | |
| D. | 取已配制好的食盐溶液时,有少量溶液洒在瓶外 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com