
��12�֣������������ճ������г��ø�����ϴ����
���� | ϴ���� | ����� | ¯������ | ������Ư | ���ձ�ը�� |
��Ʒ��ʽ |
|
|
|
|
|
��Ч�ɷ� ���� | ��ϴ���� | ���� | �������� | �������� | ��̼���� |
��1������ʹ��ϴ������ϴ�;��ϵ����ۣ�������Ϊ������ �Ĺ��ܡ�
��2������������ʣ�����ʹ�ý������� ����ĸ��ţ���
A������ B��ˮ������Ҫ�ɷ�Ϊ̼��ƺ�������þ��
C������ D��������ԭ����ͭʵ����Թ��ڱڲ����ĺ�ɫ����
��3�������ձ�ը�Ρ�����ˮ�������Na2CO3��H2O2������ը������ˮ���ټ��������Ľ���飬������ʹ����ʯ��ˮ����ǵ����壬��һ��Ӧ��������ͼ�� ��ѡ��٢ڢۢܣ����ʹ�ϵ��
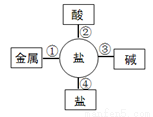
��4������������¯�������У���ͼ����ʾ��
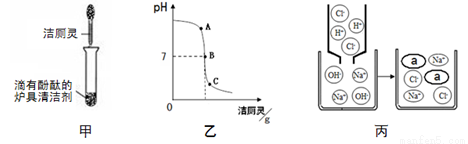
������Ӧ����Һ�ʺ�ɫ����Ӧ����Һ�е������ǣ���̪���⣩ ����ʱ��Һ����ͼ���� �㴦��ѡ��A��B��C����ʾ��
������Ӧ����ҺpHΪ7��ͼ����a������ѧʽΪ ��
��5���١�������Ư��������Ưϴ���ɱ�������ȣ�ԭ��������Ч�ɷֹ�����������к��С�������������O��O�������ݴ��Ʋ⣬���������У�������ɱ������������ (�����)��

����������Һ������ҽ��������ij��ȤС��Ϊ�ⶨһƿ���õ�ҽ�ù���������Һ��������������������ȡ����Һ51g�����������������̣����������������뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ���Լ���ù���������Һ�����ʵ�����������

��д��������̣�
��1���黯��2��AB ��3���ڣ�4����NaCl NaOH�� A ��H2O ��5����D ��2%
��������
�����������1������ʹ��ϴ������ϴ�;��ϵ����ۣ�������Ϊ�������黯���ܣ���2����Ϊ������к������ᣬ�ʿ������ᷴӦ��Ϊ���⡢ˮ������3�������ձ�ը�Ρ�����ˮ�������Na2CO3��H2O2������ը������ˮ���ټ��������Ľ���飬������ʹ����ʯ��ˮ����ǵ����壬��һ��Ӧ��������ͼ�������ᷴӦ����4��������Ӧ����Һ�ʺ�ɫ��˵����Һ�ʼ��ԣ���Ӧ����Һ�е������ǣ���̪���⣩NaCl NaOH����ʱ��Һ����ͼ����A���ʾ��������Ӧ����ҺpHΪ7��ͼ����a������ѧʽΪH2O����5���١�������Ư��������Ưϴ���ɱ�������ȣ�ԭ��������Ч�ɷֹ�����������к��С�������������O��O�������ݴ��Ʋ⣬���������У�������ɱ������������D��
��[��]�裺����������Һ�����ʵ�����ΪX
2H2O2 MnO22H2O+ O2 �� ����1��
68 32
X 0.48g
68/32 = X/0.48g ����1�� X = 1. 02g ���� 1��
����������Һ�����ʵ��������� = 1.02g / 51g �� 100% = 2% ���� 1��
�𣺹���������Һ�����ʵ���������2%������ �輰�� �ϼ�1��
���㣺�ᡢ��ε����ʡ���ѧ����ʽ�ļ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�Ͼ����ػ����п�һģ��ѧ�Ծ��������棩 ���ͣ�ѡ����
������һЩ�������ʵ�pH����ͼ��ʾ��

���������У������Ե���
A������֭ B������ C������ˮ D��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�Ͼ����������п���ģ��ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ʳƷ�е�Ӫ���أ�����Ϊ�����ṩ��������
A�������� B��ά���� C������ D����֬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�Ͼ�����ˮ���п���һ�ε��л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪������������������Ļ�ѧʽΪC12H7Cl3O2 ����������˵������ȷ����
A���������к���̼���⡢�ȡ�������Ԫ��
B���������������
C����������̼���⡢�ȡ���Ԫ�ص�������Ϊ12��7��3��2
D����������̼Ԫ�ص������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�Ͼ�����ˮ���п���һ�ε��л�ѧ�Ծ��������棩 ���ͣ�ѡ����
���á� ����ʾ��ԭ�ӣ��á�
����ʾ��ԭ�ӣ��á� ����ʾ��ԭ�ӣ���ˮ�Ļ�ѧ���ʵ����ӿɱ�ʾΪ
����ʾ��ԭ�ӣ���ˮ�Ļ�ѧ���ʵ����ӿɱ�ʾΪ
A�� B��
B�� C��
C�� D��
D��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�Ͼ�����ˮ���п���ģ��ѧ�Ծ��������棩 ���ͣ������
��4�֣�����������������У�ѡ����Ӧ���ʵ������ĸ��գ�
A.���� B.���� C.������̼ D.�������� E.�������� F.pH��ֽ
��1�������к����������� �� ��2�����òⶨ��Һ�����ȵ��� ��
��3���������Ʒ�������ֽ�ȹ�ҵ�ļ� �� ��4�����������������Ե�����___ _ __��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�Ͼ�����ˮ���п���ģ��ѧ�Ծ��������棩 ���ͣ�ѡ����
����X��һ����Ҫ����ȼ����������������(Sb2O3)����X�Ļ�ѧ����ʽΪ
Sb2O3 + 2H2O2 == X + 2H2O������X�Ļ�ѧʽΪ
A��SbO2 B��Sb2O5 C��HSbO3 D��H3SbO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�Ͼ��н������п���ģ��ѧ�Ծ��������棩 ���ͣ�ѡ����
����ˮ�д��������һ��������
A��H����NH4����Cl�� B��K����H����HCO3��
C��H����Na����OH�� D��Fe3����NO3����OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�Ͼ����п��ڶ���ģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ�С�������ʾ���������ʼ���һ�������¿��Է�����Ӧ����������ʾ����һ�������¿���ij������ֱ�ӷ�Ӧ���ɱ����±�����ѡ���У�����ͼ��Ҫ�����

| �� | �� | �� | �� |
A | BaCl2 | CuSO4 | Ba(OH)2 | HCl |
B | O2 | CO | Fe3O4 | C |
C | Fe | CuCl2 | Mg | HCl |
D | Cu | HCl | CuO | Mg |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com