
 2NaOH+H2↑+Cl2↑),这种工业成为“氯碱工业”,某研究性学习小组对该厂生产的烧碱样品进行如下探究.
2NaOH+H2↑+Cl2↑),这种工业成为“氯碱工业”,某研究性学习小组对该厂生产的烧碱样品进行如下探究.| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁. | 试管外壁发热 | 原因是______ |
| ②向①所得的溶液中逐渐加入稀硝酸至过量 | 一开始无明显现象,一段时间后产生能使澄清石灰水浑浊的气体 | 样品中含有的杂质是______ |
| ③向②所得的溶液中滴加几滴硝酸银溶液 | 产生白色沉淀 | 样品中还含有的杂质是______ |
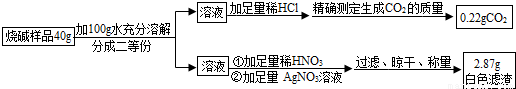
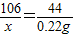 x=0.53g
x=0.53g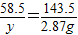 ,y=1.17g
,y=1.17g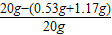 ×100%=91.5%,
×100%=91.5%,

 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:初中化学 来源: 题型:
| ||
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量烧碱样品置于试管中加水溶解,并用手触摸试管外壁 | 试管外壁发热 | 原因是 氢氧化钠固体溶于水放热 氢氧化钠固体溶于水放热 |
| ②向①所得的溶液中逐渐加入稀硝酸至过量 | 一开始无明显现象,一段时间后产生能使澄 清石灰水浑浊的气体 | 样品中含有的杂质是 碳酸钠 碳酸钠 |
| ③向②所得的溶液中滴加几滴 AgNO3 AgNO3 (化学式)溶液 |
产生白色沉淀 | 样品中还含有的杂质是_ 氯化 氯化 钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁. | 试管外壁发热 | 原因是 氢氧化钠固体溶于水放热 氢氧化钠固体溶于水放热 |
| ②向①所得的溶液中逐渐加入稀硝酸至过量 | 一开始无明显现象,一段时间后产生能使澄清石灰水浑浊的气体 | 样品中含有的杂质是 碳酸钠 碳酸钠 |
| ③向②所得的溶液中滴加几滴硝酸银溶液 | 产生白色沉淀 | 样品中还含有的杂质是 氯化钠 氯化钠 |

查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量的烧碱样品置于试管中加水溶解,用手触摸试管外壁. | 试管外壁发热 | 原因是 氢氧化钠溶于水时放出热量 氢氧化钠溶于水时放出热量 |
| ②向①所得的溶液中加入盐酸至过量. | 开始时无明显现象,过一段时间后有气泡产生. | 说明样品中含有杂质 Na2CO3 Na2CO3 |
| ③向②所得的溶液中加入硝酸银溶液. | 有白色沉淀产生. | AgNO3+NaCl═AgCl↓+NaNO3 说明样品中含有杂质氯化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁. | 试管外壁发热 |
原因是 氢氧化钠固体溶于水放热 氢氧化钠固体溶于水放热 |
| ②向①所得的溶液中逐滴加入稀硝酸至过量 | 一开始无明显现象,一段时间后产生能使澄清石灰水变浑浊的气体. | 样品中含有的杂质是 碳酸钠 碳酸钠 |
| ③向②所得的溶液中滴加几滴硝酸银溶液 | 产生白色沉淀 | 样品中还含有的杂质是 氯化钠 氯化钠 |

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁 | 试管外壁发热 | 原因是 |
| ②向①所得的溶液中逐渐加入稀硝酸至过量 | 一开始无明显现象,一段时间后产生能使澄清石灰水浑浊的气体 | 样品中含有的杂质是 |
| ③向②所得的溶液中滴加几滴硝酸银溶液 | 产生白色沉淀 | 样品中还含有的杂质是 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com