
【题目】A、B、C、D、E四种物质分别依次属于单质、氧化物、酸、碱和盐,已知B为红棕色固体,C为一种挥发性酸,D常用于改良酸性土壤,F与B属于同类物质,其相互反应情况如下图所示(短线“一”相连的物质间能反应,箭头“→”表示物质间存在着相应的转化关系(部分反应物、生成物及反应条件已略去)。请回答:
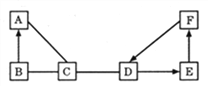
(1)A的化学式为_______________;
(2)写出下列反应或转化的化学方程式:
B与C反应:_____________________________________________;
D转化为E:______________________________________________;
(3)写出F的一种用途:__________________。
【答案】 Fe Fe2O3+6HCl=2FeCl3+3H2O Ca(OH)2+CO2=CaCO3↓+H2O 作食品干燥剂(合理答案均可)
【解析】本题是框图型推断题。首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。
已知A是一种单质,B为红棕色固体且为氧化物,B能转化为A,氧化铁和一氧化碳在高温下生成铁和二氧化碳,所以B是氧化铁,A是铁;D常用于改良酸性土壤,D是氢氧化钙;C为一种挥发性酸,铁能与C反应,则C是盐酸;F与B属于同类物质,F属于金属氧化物,F能转化为氢氧化钙,氧化钙和水反应生成氢氧化钙,则F为氧化钙,E能转化为氧化钙且E是盐,氢氧化钙能转化为E,碳酸钙高温煅烧生成氧化钙和二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙白色沉淀和水,则 E是碳酸钙。因此:
(1)A是铁,化学式为Fe;
(2)B与C的反应是氧化铁与盐酸反应生成氯化铁和水,化学方程式是:Fe2O3+6HCl=2FeCl3+3H2O;D转化为E的反应是二氧化碳和氢氧化钙反应生成碳酸钙白色沉淀和水,化学方程式是:Ca(OH)2+CO2=CaCO3↓+H2O;
(3) F是氧化钙,可用作食品干燥剂(合理答案均可)。


 口算能手系列答案
口算能手系列答案科目:初中化学 来源: 题型:
【题目】逻辑推理是化学学习常用的思维方法,下列推理不正确的是( )
A. 碱的溶液呈碱性,呈碱性的溶液不一定是碱溶液
B. 置换反应一定有单质生成,有单质生成的反应不一定是置换反应
C. 氧化物中一定含氧元素,含氧元素的化合物一定是氧化物
D. 单质中只含有一种元素,则只含有一种元素的纯净物一定是单质
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列图示,回答相关问题.
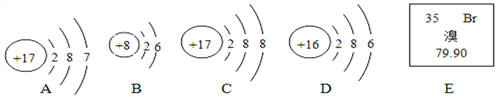
(1)A、B、C、D四种粒子中属于同种元素的是____(填字母,下同),与B的化学性质相似的是___.
(2)图E是溴元素在元素周期表的部分信息,溴的相对原子质量为_______.
(3)下图是某化学反应的微观示意图.
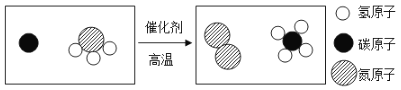
①上图中涉及的化合物有___种.
②该变化过程中不发生改变的粒子是____(填“分子”或“原子”).
③该化学反应中生成物的粒子个数比为_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】天启同学为了探究碳及其氧化物的某些性质,用如图装置进行实验:
(提示:B装置目的是为了除去杂质HCl气体)
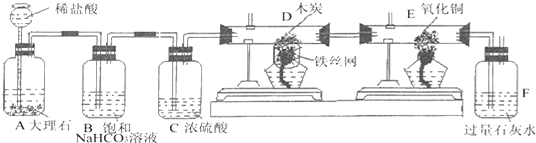
请根据如图图回答下列问题:
(1)写出下列装置中发生的化学反应方程式:E装置_________,F装置_________.
(2)D装置中发生的化学反应的基本反应类型_______,C装置中的作用是____.
(3)该装置的不足之处是______.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】变色眼镜的玻璃里加入了溴化银(AgBr)和氧化铜。在强光照射下,溴化银分解成溴(Br2)和银,玻璃颜色变深,此反应的化学方程式为_____________________________;当光线变暗时,溴和银在氧化铜作用下,重新生成溴化银,玻璃颜色变浅,而氧化铜在变化前后质量和化学性质没有变化,则氧化铜在反应中起______作用。眼镜的铜螺丝部位常出现一层绿色物质,这是由于铜生锈的原因,请完成该反应的化学方程式:2Cu+O2+_______+H2O![]() Cu2(OH)2CO3。
Cu2(OH)2CO3。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国已经全面进入高铁时代,为适应提速要求,需要把短轨焊接成长轨,常用如下反应 XAl + Fe2O3 ![]() XFe + Al2O3 焊接铁轨,该反应发生后不需要持续加热就可保持高温继续进行,方便野外操作,下列说法不正确的是
XFe + Al2O3 焊接铁轨,该反应发生后不需要持续加热就可保持高温继续进行,方便野外操作,下列说法不正确的是
A. 该反应方程式中的X 为3 B. Al2O3 属于氧化物
C. 该反应为置换反应 D. 该反应会放出大量的热
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学实验小组对 “影响石灰石与盐酸反应速率的因素——盐酸的浓度和石灰石的颗粒大小等”进行了如下实验探究,请你参与。
[进行实验]室温下,选用20mL不同溶质质量分数的盐酸(4%和6%)分别与1g颗粒状或块状的石灰石进行实验(固定夹持仪器略去)。
(1)石灰石与盐酸反应的化学方程式为___________________。
(2)按如图装置进行实验,在装药品前应检查该装置的气密性,具体的做法是____。
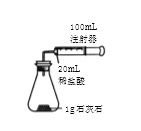
开始实验时,应将20mL稀盐酸_____________(填“快速”或“缓慢”)推入锥形瓶中,以保证盐酸能全部推入锥形瓶中。
[处理数据](3)实验小组进行实验后,获得的相关实验数据如表所示:
实验 编号 | 盐酸的溶质质量分数 (均取20mL) | 石灰石固体形状 (均取1g) | 二氧化碳的体积/mL (均收集前30s的气体) |
a | 4% | 颗粒 | 64.0 |
b | 4% | 块状 | 40.4 |
c | 6% | 颗粒 | 98.2 |
d | 6% | 块状 | 65.3 |
①要比较不同溶质质量分数的盐酸对反应速率的影响,可选择的实验编号是_______(写一组),由此可得到的结论是_______________。
②从上述实验得出石灰石的颗粒大小对反应速率影响的结论是_____________。
(4)如表是实验时记录生成的二氧化碳气体的体积和对应的时间的一组实验数据(每间隔4s读数一次):
时间/s | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | 36 | 40 | |
气体体积/mL | 16.0 | 22.2 | 29.4 | 39.3 | 50.4 | 57.6 | 62.0 | 64.7 | 66.0 | 66.0 |
从上表数据可以分析得出,到20s后反应速率逐渐变____,其主要原因是___。
(5)你认为影响石灰石与盐酸反应速率的因素还有____,请设计实验方案验证你的猜想:____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图中,①是钠元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图。试回答下列问题:
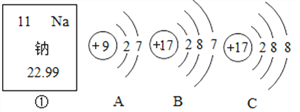
(1)钠元素的原子序数为______;
(2)A、B、C中属于同种元素的粒子是_________(填字母编号);
(3)A和B两种粒子的_________________相同,所以它们有相似的化学性质;
(4)C所表示的粒子是_______________(填“原子”或“离子”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合下图回答问题:
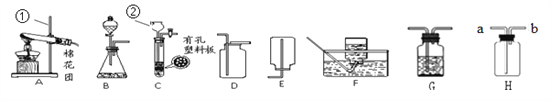
(1)写出图中有标号仪器的名称:①__________,② ___________。
(2)用加热高锰酸钾的方法制取氧气,应选用的发生装置是(填字母编号)_______,装入药品前应先_______,写出该反应化学方程式_____________________。
(3)用B、D装置组合制取二氧化碳气体的化学方程式___________________________。 若要获得干燥的该气体,除发生、收集装置外,还应选用G装置,并在该装置中盛放_______(填名称)。如果用H装置收集该气体,则气体从_______________端进入(填“a”或“b”)。
(4)实验室用锌粒和稀硫酸反应制取H2的化学方程式___________________,常选用装置B或C, C与B相比较,C的优点是_______________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com