
 酸、碱、盐是有广泛用途的重要化合物.某化学活动小组的同学围绕这几类化合物进行了一系列的探究活动.
酸、碱、盐是有广泛用途的重要化合物.某化学活动小组的同学围绕这几类化合物进行了一系列的探究活动.| 实验目的 | 实验操作 | 现象 | 结论或化学方程式 |
除去碳酸钠 | 取少量该固体样品溶于水配成溶液,滴加适量的氯化钡溶液,充分反应后过滤 | 有白色沉淀生成 | 有关反应的化学方程式为Na2CO3+BaCl2=BaCO3↓+2NaCl |
| 检验是否含有氢氧化钠 | 在滤液中滴加酚酞溶液 | 溶液变红 | 该样品中含有氢氧化钠 |
分析 (1)根据溶液稀释前后溶质的质量不变来求算出需要加入水的质量,根据浓硫酸的密度和水的密度比较及浓硫酸溶解放出大量的热来分析不能将水注入浓硫酸的原因;利用碳酸盐的性质,检验碳酸钠的存在,证明氢氧化钠变质;
(2)选择合适的试液检验氢氧化钠是否存在;碳酸钠能与氯化钡反应形成白色沉淀,可以判断出反应产生现象,然后利用氢氧化钠能使酚酞变红的性质,再向反应后溶液中滴加酚酞试液,观察溶液颜色,以确定溶液的组成,从而判断氢氧化钠变质情况
解答 解:(1)根据溶液稀释前后溶质的质量不变,设需加入水的质量为x,则:
10g×98%=(10g+x)×20%
解得:x=39g,
由于浓硫酸的密度比水的大,并且浓硫酸在溶解的时候要放出大量的热,放出的热足以使水沸腾,而引起酸液的迸溅,所以为了防止酸液迸溅引起危险,而应该将浓硫酸慢慢注入水中,并不断搅拌;
故填:39;浓硫酸的密度比水的大,并且浓硫酸在溶解的时候要放出大量的热,放出的热足以使水沸腾,而引起酸液的迸溅,所以为了防止酸液迸溅引起危险,而应该将浓硫酸慢慢注入水中,并不断搅拌;
(2)①碳酸盐可以与酸反应放出能使澄清石灰水变浑浊的二氧化碳气体;所以无色溶液可能是:盐酸;故填:盐酸;
②氯化钡溶液与碳酸钠溶液反应生成碳酸钡沉淀和氯化钠,所以根据题中的实验结论可以知道能观察到的现象为:有白色沉淀生成,有关反应的化学方程式为:Na2CO3+BaCl2=BaCO3↓+2NaCl,而氯化钠、氯化钡溶液都呈中性;故在反应后的溶液中滴入酚酞,溶液变红色,则一定是氢氧化钠溶液使酚酞变红,所以氢氧化钠没有完全变质;
故填:
| 实验目的 | 实验操作 | 现象 | 结论或化学方程式 |
| 除去碳酸钠 | 取少量该固体样品溶于水配成溶液,滴加适量的 氯化钡溶液,充分反应后过滤 | 有白色沉淀生成 | 有关反应的化学方程式为 Na2CO3+BaCl2=BaCO3↓+2NaCl |
| 检验是否含有氢氧化钠 | 在滤液中滴加酚酞溶液 | 溶液变红 | 该样品中含有氢氧化钠 |
点评 检验氢氧化钠与碳酸钠的混合物时,可先把碳酸钠变成沉淀并且不生成影响氢氧化钠检验的碱性物质,然后使用酚酞检验氢氧化钠.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 催化剂都能加快化学反应速率 | |
| B. | 含氧元素的化合物都是氧化物 | |
| C. | 物质发生化学变化时都伴随着能量的变化 | |
| D. | 只有燃烧的化学反应才能放出热量 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 下表是a、b二种物质在不同温度时的溶解度,请根据表中数据回答:
下表是a、b二种物质在不同温度时的溶解度,请根据表中数据回答:| 温度/℃ | 0 | 20 | 30 | 40 | 60 | |
| 溶解度/g | 物质a | 13.3 | 31.6 | 45.8 | 63.9 | 110 |
| 物质b | 21.4 | 9.84 | 7.24 | 5.63 | 3.87 | |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
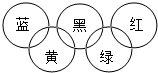 奥运会会标是五环旗,假定奥运五环旗中的一环表示一种物质,相连环物质间一定条件下能发生常见反应,不相连环物质间不能发生反应,且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组是( )
奥运会会标是五环旗,假定奥运五环旗中的一环表示一种物质,相连环物质间一定条件下能发生常见反应,不相连环物质间不能发生反应,且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组是( )| 蓝 | 黄 | 黑 | 绿 | 红 | |
| A | SiO2 | NaOH溶液 | CuSO4溶液 | Ag | O2 |
| B | O2 | Fe | 稀H2SO4 | NaOH溶液 | CO2 |
| C | O2 | NH3 | 稀H2SO4 | NaOH溶液 | Al(OH)3 |
| D | Mg | Al | CO2 | Fe2O3 | KOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
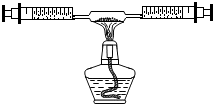 某课外活动小组在学习了书本“空气中氧气含量的测定”实验,知道P2O5不能随便排放在空气中,否则会对空气造成污染,所以对该实验进行了改进:
某课外活动小组在学习了书本“空气中氧气含量的测定”实验,知道P2O5不能随便排放在空气中,否则会对空气造成污染,所以对该实验进行了改进:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
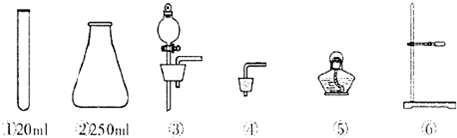
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com