
| A. | C24H38O4是由24个碳原子、38个氢原子、4个氧原子构成的有机物 | |
| B. | C24H38O4中碳、氢、氧元素三种元素的质量比为12:19:2 | |
| C. | C24H38O4中氢元素质量分数最小 | |
| D. | 邻苯二甲酸二辛酯是无机化合物 |
分析 A.根据物质的结构来分析;
B.根据元素质量比的计算方法进行计算;
C.根据元素质量比进行计算;
D.根据无机物与有机物的概念来分析.
解答 解:A.邻苯二甲酸二辛酯是由邻苯二甲酸二辛酯分子构成的,而不是由原子直接构成的,故错误;
B.邻苯二甲酸二辛酯中碳、氢、氧元素的质量比为:(12×24):(1×38):(16×4)=144:19:32;故错误;
C.邻苯二甲酸二辛酯中碳、氢、氧元素的质量比为:(12×24):(1×38):(16×4)=144:19:32,可见其中氢元素的质量分数最小;故正确;
D.含有碳元素的化合物为有机化合物,邻苯二甲酸二辛酯含有碳元素,故属于有机化合物,故错误.
故选C.
点评 本题主要考查化学式的意义、根据化学式确定组成物质元素之间的质量关系以及有机物的定义,掌握了这些问题就不难解决此题了.


科目:初中化学 来源: 题型:实验探究题
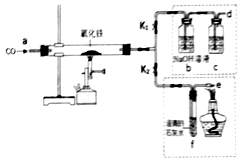 如图是化学兴趣小组成员用一氧化碳还原氧化铁实验作了绿色化改进后制取单质铁的装置.
如图是化学兴趣小组成员用一氧化碳还原氧化铁实验作了绿色化改进后制取单质铁的装置.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A化学之最 | B化学与生活 |
| ①熔点最低的金属是汞 ②地壳中含量最高的金属元素是铁 | ①区分硬水和软水:可用肥皂水 ②水壶中的水垢:可加食盐水浸泡除去 |
| C物质保存方法及解释 | D化学与工农业 |
| ①浓盐酸密封保存:防止挥发 ②氢氧化钠密封保存:防止潮解、变质 | ①用焦炭和铁矿石炼铁 ②施用过量化肥、农药增加粮食产量 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题


查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | t1℃时,a、c两种物质的溶液中溶质的质量分数相同 | |
| B. | t2℃时,a、b、c三种物质的溶解度由大到小的顺序为a>b>c | |
| C. | 将等质量的三种物质的饱和溶液分别由t2℃降温到t1℃,a溶液中析出的晶体质量最大 | |
| D. | 当a中含有少量b时,可以用降温结晶的方法提纯a |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 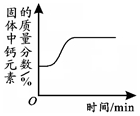 高温煅烧一定质量的碳酸钙 | |
| B. |  向一定量铁粉中加入稀盐酸 | |
| C. | 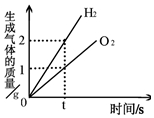 电解水时,反应时间与生成气体的质量关系 | |
| D. | 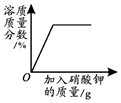 向接近饱和的硝酸钾溶液中加硝酸钾固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 解释或结论 |
| (1)将清新洁净的空气通过NaOH溶液,再通过浓硫酸. | 通过浓硫酸的目的是为了除去空气中的水蒸气. |
| (2)将气体通过能与氧气反应的物质(提示:反应不能生成新的气体). | 请写出能用于除去氧气的物质名称:红磷、白磷、铜等. |
| (3)收集剩余气体,并测定该气体的密度. | 密度:1.257 2g˙L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com