
科目:初中化学 来源: 题型:选择题
| A. | 分别将样品摔在瓷砖上,均没碎裂 | |
| B. | 分别将样品在强光下照射,不透明的是聚酯塑料 | |
| C. | 分别将样品用铁制小刀刻画,没有痕迹留下的是有机玻璃 | |
| D. | 分别将样品在酒精灯火焰上灼烧一会儿,没有变化的是玻璃 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
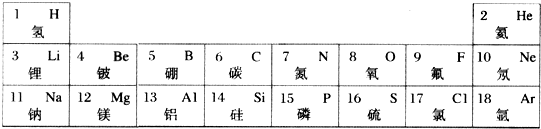
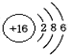 ,在化学反应中易得到电子(选填“得到”或“失去”),形成S2-(填 粒子符号).
,在化学反应中易得到电子(选填“得到”或“失去”),形成S2-(填 粒子符号).查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 熔点 | 沸点 | 热稳定性 | 其他 |
| 101℃~102℃ | 150℃~160℃升华 | 100.1℃分解出水,175℃分解成CO2、CO、H2O | 与 Ca(OH)2反应产生白色沉淀(CaC2O4) |

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
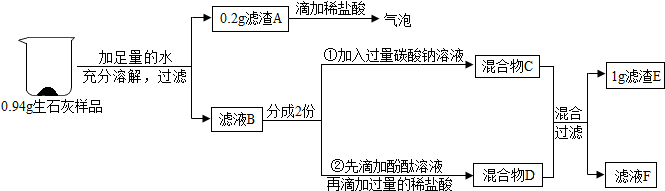
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com